Diflucan (Fluconazol)

Dosis
Diflucan 50 mg
| Cantidad | Precio por comprimido | Precio total | |
|---|---|---|---|
| 60 | €0,81 | €48,48 | |
| 90 | €0,72 | €64,65 | |
| 120 | €0,67 | €80,81 | |
| 180 | €0,63 | €113,98 | |
| 270 | €0,61 | €164,17 | |
| 360 | €0,59 | €211,80 |
Diflucan 100 mg
| Cantidad | Precio por comprimido | Precio total | |
|---|---|---|---|
| 30 | €1,45 | €43,38 | |
| 60 | €1,09 | €65,50 | |
| 90 | €0,97 | €87,61 | |
| 120 | €0,91 | €109,73 | |
| 180 | €0,85 | €153,11 | |
| 270 | €0,81 | €218,60 |
Diflucan 150 mg
| Cantidad | Precio por comprimido | Precio total | |
|---|---|---|---|
| 30 | €1,84 | €55,29 | |
| 60 | €1,38 | €82,51 | |
| 90 | €1,22 | €109,73 | |
| 120 | €1,15 | €137,80 | |
| 180 | €1,07 | €192,24 | |
| 270 | €1,02 | €274,74 |
Diflucan 200 mg
| Cantidad | Precio por comprimido | Precio total | |
|---|---|---|---|
| 30 | €2,89 | €86,76 | |
| 60 | €2,10 | €125,89 | |
| 90 | €1,82 | €164,17 | |
| 120 | €1,69 | €203,29 | |
| 180 | €1,55 | €279,85 | |
| 270 | €1,47 | €397,23 |
Diflucan 400 mg
| Cantidad | Precio por comprimido | Precio total | |
|---|---|---|---|
| 30 | €4,82 | €144,60 | |
| 60 | €3,62 | €216,90 | |
| 90 | €3,22 | €290,05 | |
| 120 | €3,03 | €363,21 | |
| 180 | €2,83 | €508,66 | |
| 270 | €2,69 | €726,41 |
Pago y envío
Tu pedido se prepara con cuidado y se envía en un plazo de 24 horas. Así es como suele ser el paquete.
Tiene el tamaño de una carta personal normal (24x11x0,7 cm), sin ninguna indicación sobre su contenido.



| Método de envío | Plazo de entrega |
|---|---|
| Exprés Gratis desde €300,00 | Entrega estimada en España: 4-7 días |
| Estándar Gratis desde €200,00 | Entrega estimada en España: 14-21 días |









Cupones de descuento
- Día de Año Nuevo - 1 de enero de 2026 9% ANONUEVO9
- Día de Reyes - 6 de enero de 2026 10% REYES10
- Día del Trabajo - 1 de mayo de 2026 6% TRABAJO6
- Asunción - 15 de agosto de 2026 6% ASUNCION6
- Fiesta Nacional de España - 12 de octubre de 2026 7% NACIONAL7
- Día de Todos los Santos - 1 de noviembre de 2026 6% SANTOS6
- Día de la Constitución - 6 de diciembre de 2026 7% CONSTITUCION7
- La Inmaculada Concepción - 8 de diciembre de 2026 6% INMACULADA6
- Nochebuena - 24 de diciembre de 2026 9% NOCHEBUENA9
- Navidad - 25 de diciembre de 2026 10% NAVIDAD10
- Nochevieja - 31 de diciembre de 2026 8% NOCHEVIEJA8
Nombres de marca
| País | Nombres de marca |
|---|---|
 Alemania Alemania | Canex Canifug Fluco Fluc Flucobeta Flucoderm FlucoLich Flunazul Fungata |
 Argentina Argentina | Candimicol Damicol Femixol Flucoginkan Fluconovag Fluzol Fungicil Fungocina Fungototal Honguil Plus Klonarizol Klonazol Micolis Novo Mutum Naxo C Nifurtox Niofen Periplum Ponaris Proseda F Triflucan |
 Australia Australia | Dizole Fluzole Ozole |
 Brasil Brasil | Candix Candizol Celozol Farmazol Floltec Flucanil Flucanol Flucazol Flucocin Flucodan Flucoltrix Flucomed Fluconal Fluconax Fluconeo Fluconid Flucozen Flucozix Flunal Flunazol Fluotec Flusan Flutec Fungnon Glyflucan Helmicin Lertus Monipax Pantec Pronazol Riconazol Teczol Triazol Unizol Zelix Zolanix Zolmic Zolstatin Zoltec Zoltren |
 Bélgica Bélgica | Candizole Fungimed |
 Dinamarca Dinamarca | Conasol Fungal |
 España España | Citiges Lavisa Loitin Nesporac Solacap |
 Francia Francia | Beagyne Triflucan |
 Grecia Grecia | Azoflu Azzol-S Dalrich Falipan Farviron Figalol Flucalit Flucocaps Flucodrug Flucofin Fluconapen Flucoran Flucozol Flukatril Flusenil Fluzomic Fumecal Funadel Fungo Fungram Fungustatin Fungusteril Fuxilidin Gynosant Hadlinol Medoflucon Mycazole Neomycol Opumyk Rifagen Stabilanol Tierlite Varmec Zidonil |
 Hungría Hungría | Dermyc Diflazon Flucohexal Flucoric Mycosyst Nofung |
 Italia Italia | Biozolene Elazor Flumicon Lefunzol Riflax Winch |
 Malasia Malasia | Avezol Biozole Flucon Fluconol Flucoric Flugal Fukole Medoflucon Odaft Stalene Zolstan |
 México México | Afungil Bioxel Candizol Difusel Fectrin Fharder Fleridux Flucoxan Fludisol Fluhexal Flukenol Flukezol Fluxes Fluxicap Fluzor Funser Lanfluzol Menifar Neofomiral Ongicil Oxifungol Ranflu Solarisol Terplex Waynazol Zilrin Zoldicam Zonal |
 Nueva Zelanda Nueva Zelanda | Canesten Fluconazole Flucazole |
 Países Bajos Países Bajos | Flucoderm |
 Polonia Polonia | Flucofast FlucoLEK Fluconazin Flumycon Mycomax Mycosyst |
 Portugal Portugal | Azoflune Fludocel Maxflin Reforce Supremase |
 República Checa República Checa | Diflazon Fluco Forcan Mycomax Mycosyst Mykohexal |
 Turquía Turquía | Biocanol Candidin Flucan Fluzole Fungan Kandizol Lumen Triflucan Trizol Zolax |
| Fabricante | Nombres de marca |
|---|---|
| Cipla Limited | FCN Flucalup Forcan FZ |
| Inc. | FCN Flucalup Forcan FZ |
| Intas Pharmaceuticals Ltd. | FCN Flucalup Forcan FZ |
| Lupin Pharmaceuticals | FCN Flucalup Forcan FZ |
| Zenlabs Pharmaceutical Inc. | FCN Flucalup Forcan FZ |
Descripción
El fluconazol es un antifúngico ampliamente utilizado para tratar infecciones por levaduras y otros hongos, ya que frena su crecimiento en el organismo. Está disponible en distintas dosis y suele recetarse cuando se necesita un tratamiento oral eficaz y cómodo.
Usos
Antes de comprar fluconazol en línea, lea información importante sobre este medicamento.
El fluconazol se usa para tratar la candidiasis orofaríngea, esofágica o vulvovaginal, así como otras infecciones candidiásicas sistémicas graves, como infecciones urinarias, peritonitis, candidemia, candidiasis diseminada, meningitis o neumonía. También se utiliza para tratar la meningitis causada por Cryptococcus neoformans y para tratar blastomicosis, coccidioidomicosis e histoplasmosis.

El fluconazol también se ha utilizado en infecciones menos graves, como micosis superficiales, dermatofitosis y onicomicosis. Además, se emplea para prevenir infecciones fúngicas graves, como coccidioidomicosis, criptococosis o candidiasis mucocutánea, en personas con infección por el virus de la inmunodeficiencia humana (VIH) y en otros pacientes inmunodeprimidos, por ejemplo, personas con cáncer o trasplante de médula ósea.
Antes de empezar el tratamiento con fluconazol, deben obtenerse muestras adecuadas para cultivo fúngico y otras pruebas de laboratorio relevantes, como serología o histopatología, para aislar e identificar el organismo causante. El tratamiento con fluconazol puede iniciarse mientras se esperan los resultados de estas pruebas in vitro; sin embargo, cuando estén disponibles, debe ajustarse en consecuencia. Si se realizan pruebas de sensibilidad in vitro al fluconazol, los resultados deben interpretarse con cautela, ya que las pruebas disponibles en la actualidad pueden no reflejar con exactitud la actividad in vivo del fluconazol.
Infecciones candidiásicas
Candidiasis orofaríngea y esofágica
El fluconazol por vía oral o intravenosa se utiliza para tratar la candidiasis orofaríngea en adultos inmunodeprimidos con síndrome de inmunodeficiencia adquirida (SIDA), complejo relacionado con el SIDA avanzado (ARC), cáncer u otra enfermedad subyacente grave. También se usa por vía oral o intravenosa para tratar la candidiasis esofágica en adultos con SIDA, cáncer u otras enfermedades graves de base, incluida la esclerosis sistémica progresiva.
El fluconazol parece ser al menos tan eficaz y, en algunos casos, más eficaz que otros antifúngicos usados en el tratamiento inicial de las infecciones candidiásicas orofaríngeas y/o esofágicas. Se considera un tratamiento de elección para estas infecciones.
El fluconazol ha logrado la resolución clínica de los signos y síntomas de la infección en el 79-100 % de los pacientes con candidiasis orofaríngea; sin embargo, las curaciones microbiológicas suelen alcanzarse en el 44-87 % de los casos, y la tasa de recaída puede ser alta, especialmente en pacientes neutropénicos. En adultos con candidiasis esofágica confirmada por endoscopia, el fluconazol ha conseguido la resolución clínica de los signos y síntomas en aproximadamente el 61-93 % de los pacientes. En un estudio en adultos con candidiasis esofágica y esclerosis sistémica progresiva, el tratamiento con fluconazol produjo curaciones micológicas en aproximadamente el 93 % de los pacientes en 2-4 semanas. Sin embargo, la tasa de recaída fue de casi el 100 % en los 3 meses siguientes a la suspensión del tratamiento con fluconazol.
Los pacientes con VIH que presentan episodios graves o recurrentes de candidiasis orofaríngea o esofágica pueden beneficiarse de un tratamiento supresor o de mantenimiento a largo plazo (profilaxis secundaria) para prevenir recaídas.
Algunos clínicos consideran que el tratamiento tópico con clotrimazol oral o nistatina oral es la opción de elección para la candidiasis orofaríngea no complicada en personas con VIH y recomiendan reservar los antifúngicos sistémicos, como fluconazol oral, itraconazol oral o ketoconazol oral, para los casos que no responden al tratamiento tópico y para la candidiasis orofaríngea grave con afectación esofágica. Sin embargo, otros prefieren usar desde el inicio un antifúngico azólico oral.
El fluconazol oral o la solución oral de itraconazol son al menos tan eficaces como el tratamiento tópico. En un estudio con adultos con VIH y candidiasis orofaríngea, la tasa de respuesta y la tasa de erradicación micológica a los 14 días de tratamiento fueron del 100 y 75 %, respectivamente, en quienes recibieron fluconazol oral (100 mg una vez al día), y del 65 y 20 %, respectivamente, en quienes recibieron clotrimazol tópico (pastilla oral de 10 mg 5 veces al día). En otro estudio, 14 días de tratamiento con fluconazol oral (100 mg una vez al día como suspensión oral) fueron más eficaces que 14 días con nistatina tópica (500.000 unidades como suspensión oral 4 veces al día). La tasa de curación micológica fue del 60 % en el grupo de fluconazol y del 6 % en el grupo de nistatina, y la tasa de recaída a los 42 días fue del 27 y 11 %, respectivamente. Tras un seguimiento prolongado, la comparación de la eficacia entre fluconazol y otros antifúngicos requiere más estudios.
El tratamiento antiinfeccioso sistémico es necesario para la candidiasis esofágica. Algunos clínicos señalan que un régimen de 14 a 21 días con fluconazol oral (100 mg una vez al día) o solución oral de itraconazol (200 mg una vez al día) es muy eficaz para tratar la candidiasis esofágica, mientras que el ketoconazol oral resulta menos eficaz. Estos clínicos sugieren usar solución oral de itraconazol en pacientes que no responden al fluconazol oral. La anfotericina B intravenosa puede utilizarse en pacientes con enfermedad refractaria. En un estudio multicéntrico, aleatorizado y doble ciego que comparó fluconazol oral (dosis inicial de 100 mg/día, aumentada a 200 mg/día si no había mejoría en 1-2 semanas) durante 8 semanas con ketoconazol oral (dosis inicial de 200 mg/día, aumentada a 400 mg/día si no había mejoría en 1-2 semanas) en pacientes con SIDA y candidiasis esofágica confirmada por endoscopia, la curación endoscópica y la resolución de los síntomas esofágicos se produjeron en el 91 y 85 % de los pacientes tratados con fluconazol, respectivamente, frente al 52 y 65 % en los tratados con ketoconazol. Otro estudio en pacientes inmunodeprimidos con candidiasis esofágica indica que quienes fueron tratados con fluconazol pueden necesitar un tiempo de tratamiento inicial más corto que quienes recibieron ketoconazol.
Candidiasis vulvovaginal
El fluconazol oral se usa para tratar la candidiasis vulvovaginal no complicada y la candidiasis vulvovaginal complicada en mujeres no embarazadas. Antes de iniciar por primera vez un tratamiento antifúngico en una mujer con signos y síntomas de candidiasis vulvovaginal no complicada, debe confirmarse el diagnóstico demostrando la presencia de levaduras o seudohifas mediante examen microscópico directo del flujo vaginal (preparación en fresco con hidróxido de potasio al 10 % [KOH] o tinción de Gram) o mediante cultivo. La identificación de Candida en cultivo en ausencia de síntomas no es una indicación de tratamiento antifúngico, ya que aproximadamente el 10-20 % de las mujeres albergan Candida u otras levaduras en la vagina. En mujeres con candidiasis vulvovaginal recurrente, deben obtenerse cultivos vaginales para confirmar el diagnóstico e identificar especies de Candida poco habituales, como C. glabrata.
Candidiasis vulvovaginal no complicada
El fluconazol oral trata eficazmente la candidiasis vulvovaginal no complicada cuando se administra en dosis única. Una dosis oral única de 150 mg de fluconazol produce curaciones clínicas, es decir, desaparición de ardor, picor, hinchazón, eritema, excoriaciones, dispareunia y/o ulceración vulvovaginal, además de una reducción notable del flujo vaginal, entre 5 y 16 días después de la dosis en aproximadamente el 90-100 % de las mujeres no embarazadas con candidiasis vulvovaginal no complicada; las curaciones micológicas se alcanzan en aproximadamente el 77-100 %. Entre 27 y 62 días después de la dosis única, las tasas de curación clínica y micológica son del 61-90 %, y la tasa de recaída, reinfección o recolonización es de aproximadamente el 23 %. Los resultados de varios estudios en pacientes con candidiasis vulvovaginal no complicada sugieren que una dosis única de 150 mg de fluconazol oral es tan eficaz como los regímenes de dosis múltiples de clotrimazol intravaginal, econazol, miconazol o terconazol. Además, el régimen oral de dosis única de fluconazol es tan eficaz como itraconazol oral o ketoconazol oral para esta afección.
En estudios controlados en pacientes con candidiasis vulvovaginal, las tasas de curación clínica y micológica a los 14 y 30-35 días fueron similares en pacientes que recibieron fluconazol oral (dosis única de 150 mg) en comparación con quienes recibieron clotrimazol intravaginal (tableta vaginal de 100 mg una vez al día durante 7 días) o miconazol (crema vaginal de 100 mg una vez al día durante 7 días). A los 14 días, la tasa de curación clínica fue de aproximadamente el 95-96 % con fluconazol y del 95-97 % con clotrimazol o miconazol intravaginal; la tasa de curación micológica fue del 77-80 % con fluconazol y del 72-82 % con clotrimazol o miconazol intravaginal. A los 30-35 días, la tasa de curación clínica fue de aproximadamente el 69-75 % con fluconazol y del 72-80 % con clotrimazol o miconazol intravaginal, y la tasa de curación micológica fue del 61-63 % con fluconazol y del 57-63 % con clotrimazol o miconazol intravaginal.
En España, la práctica clínica suele alinearse con las guías europeas y nacionales, que indican que la candidiasis vulvovaginal no complicada, definida como una infección leve o moderada, esporádica o poco frecuente, probablemente causada por C. albicans o que aparece en mujeres inmunocompetentes, puede tratarse con un antifúngico azólico intravaginal, como butoconazol, clotrimazol, miconazol, terconazol o tioconazol, administrado en dosis única o en un tratamiento corto, o con fluconazol oral en dosis única. Estos regímenes suelen asociarse con tasas de curación clínica y micológica del 80-90 % en mujeres no embarazadas y sanas con infecciones no complicadas. Algunos clínicos consideran que una dosis oral única de fluconazol puede ofrecer ventajas frente al tratamiento intravaginal convencional, porque facilita la adherencia y puede reducir o eliminar infecciones rectales concomitantes que pueden ser una fuente de reinfección. Al valorar los posibles riesgos y beneficios del tratamiento oral frente al intravaginal, debe tenerse en cuenta el potencial de toxicidad, por ejemplo hepatotoxicidad, y las interacciones medicamentosas asociadas al tratamiento oral. La incidencia de efectos secundarios es mayor en las pacientes que reciben una dosis oral única de fluconazol que en quienes reciben tratamiento intravaginal, por lo que este aspecto también debe evaluarse con cuidado.
Candidiasis vulvovaginal complicada y recurrente
El fluconazol oral trata la candidiasis vulvovaginal complicada, incluidas las infecciones recurrentes y graves. La candidiasis vulvovaginal complicada se define como infecciones recurrentes o graves, causadas por especies de Candida distintas de C. albicans o que aparecen en mujeres embarazadas o en mujeres con enfermedades de base, como diabetes no controlada, debilitamiento o inmunosupresión.
No se han establecido regímenes óptimos para el tratamiento de la candidiasis vulvovaginal recurrente, generalmente definida como 4 o más episodios sintomáticos al año. Aunque cada episodio causado por C. albicans puede responder a la dosis única habitual de fluconazol oral o a un tratamiento antifúngico intravaginal de corta duración, puede ser necesario prolongar el tratamiento inicial para lograr la remisión micológica, y también puede hacer falta un tratamiento de mantenimiento crónico para prevenir recaídas. En la práctica española y europea, un régimen inicial intensivo de 7 a 14 días con un antifúngico azólico intravaginal o un régimen de 2 dosis de fluconazol oral (150 mg repetidos 3 días después) suele ir seguido de un tratamiento de mantenimiento antifúngico administrado durante 6 meses. Para el mantenimiento, las opciones incluyen clotrimazol intravaginal (500 mg una vez por semana), ketoconazol oral (100 mg una vez al día), fluconazol oral (100-150 mg una vez por semana) o itraconazol oral (400 mg una vez al mes o 100 mg una vez al día). Estos regímenes pueden reducir eficazmente las infecciones recurrentes; sin embargo, entre el 30 y el 40 % de las mujeres vuelven a presentar la enfermedad una vez que se suspende el tratamiento de mantenimiento.
La tasa de respuesta a los regímenes antifúngicos de corta duración es menor en pacientes con candidiasis vulvovaginal grave, es decir, con eritema vulvar extenso, edema, excoriaciones y fisuras. Para estas infecciones se recomienda un régimen de 2 dosis de fluconazol oral (150 mg repetidos 3 días después) o 7-14 días de un antifúngico azólico intravaginal. Estos regímenes más prolongados también pueden ser necesarios para tratar la candidiasis vulvovaginal en mujeres con enfermedades debilitantes de base, como diabetes no controlada o tratamiento con corticosteroides. La candidiasis vulvovaginal puede aparecer con más frecuencia y ser más grave en mujeres con infección por VIH que en mujeres sin VIH. Estas infecciones se han reconocido como una manifestación temprana del síndrome de inmunodeficiencia adquirida (SIDA) en mujeres. Aunque no se ha establecido el tratamiento óptimo para la candidiasis vulvovaginal recurrente en mujeres con VIH, hasta la fecha no hay pruebas de que estas mujeres tengan una respuesta inferior a los tratamientos antifúngicos intravaginales u orales recomendados habitualmente para la candidiasis vulvovaginal. Por lo tanto, el Centros para el Control y la Prevención de Enfermedades (CDC) y otros clínicos recomiendan que el tratamiento de la candidiasis vulvovaginal en mujeres con VIH sea el mismo que en mujeres sin infección por VIH.
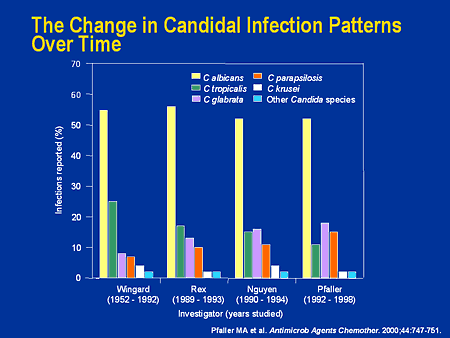
En raras ocasiones, la candidiasis vulvovaginal recurrente puede estar causada por cepas resistentes de C. albicans o, más frecuentemente, por otras especies de Candida con menor sensibilidad a los antifúngicos azólicos, como C. glabrata. Se ha sugerido que el tratamiento repetido de la candidiasis vulvovaginal recurrente con antifúngicos azólicos intravaginales, así como el uso prolongado e inadecuado de estos fármacos para la automedicación, pueden favorecer la selección de Candida resistentes a los antifúngicos azólicos. No se ha determinado el tratamiento óptimo para la candidiasis vulvovaginal causada por Candida con sensibilidad reducida a los azoles. Para la candidiasis vulvovaginal causada por especies de Candida distintas de C. albicans, en general se recomienda un tratamiento de 7 a 14 días con un antifúngico distinto del fluconazol; si hay recurrencia, puede considerarse el uso intravaginal de ácido bórico (cápsula de 600 mg una vez al día durante 2 semanas). Se recomienda la derivación a un especialista.
Candidemia y otras infecciones candidiásicas
El fluconazol ha tratado eficazmente infecciones candidiásicas graves del tracto urinario, peritonitis y neumonía. También ha sido eficaz en el tratamiento de candidiasis mucocutánea crónica, candidemia, candidiasis diseminada crónica (candidiasis hepatoesplénica), endocarditis candidiásica, meningitis candidiásica, osteomielitis candidiásica y otras infecciones candidiásicas sistémicas graves. Ha sido eficaz en el tratamiento de algunas infecciones candidiásicas que no respondieron al tratamiento con anfotericina B. El fluconazol también ha mostrado eficacia en infecciones candidiásicas potencialmente mortales en pacientes con trasplante de órganos que reciben tratamiento inmunosupresor. En algunos receptores de trasplante renal, el tratamiento con fluconazol eliminó eficazmente las infecciones fúngicas sin necesidad de suspender ni reducir la dosis de inmunosupresores.
Tanto la anfotericina B IV como el fluconazol IV u oral se consideran tratamientos de elección para la candidiasis sistémica invasiva; sin embargo, ha sido difícil identificar los regímenes antifúngicos óptimos para estas infecciones y cada fármaco presenta inconvenientes. Aunque el fluconazol puede tolerarse mejor y ser más fácil de administrar que la anfotericina B IV, cada vez se aíslan con más frecuencia cepas resistentes de C. albicans en pacientes que han recibido tratamiento previo con fluconazol, especialmente en personas con VIH. Algunas infecciones candidiásicas, como la candidemia, están siendo causadas con mayor frecuencia por cepas intrínsecamente resistentes al fluconazol, como C. krusei, o probablemente resistentes, como C. glabrata. La elección del antifúngico para el tratamiento inicial de las infecciones candidiásicas invasivas debe tener en cuenta los datos epidemiológicos locales o del centro sobre la prevalencia de las distintas cepas de Candida y sus patrones de resistencia, el estado de colonización del paciente, la gravedad y duración de la neutropenia o la inmunosupresión, y el uso previo de fluconazol. La mayoría de los clínicos recomiendan anfotericina B IV si el microorganismo causante es, o probablemente es, C. krusei; sin embargo, se prefiere fluconazol si la infección está causada por C. lusitaniae.
Dado que la candidemia se asocia con una morbilidad considerable y con riesgo de secuelas a largo plazo, en general se recomienda tratamiento antifúngico en todos los pacientes con candidemia, sean o no neutropénicos, además de retirar y/o sustituir cualquier catéter intravascular. Se ha sugerido que el fluconazol por vía oral puede preferirse a la anfotericina B por vía intravenosa para tratar la candidemia en pacientes no neutropénicos, estén clínicamente estables o no, salvo que haya evidencia de infección por cepas resistentes al fluconazol o de uso previo de este fármaco. La anfotericina B por vía intravenosa suele preferirse en casos de candidemia grave, en pacientes con infecciones causadas por cepas que pueden ser resistentes al fluconazol, como C. krusei o C. glabrata, en pacientes que han recibido fluconazol recientemente y en pacientes inmunodeprimidos, como aquellos con infección por VIH. En un estudio controlado realizado en pacientes inmunocompetentes y con un recuento normal de neutrófilos, la respuesta al tratamiento convencional con anfotericina B por vía intravenosa o con fluconazol fue similar. Ambos regímenes parecieron igualmente eficaces. La tasa global de respuesta a un régimen convencional de anfotericina B por vía intravenosa o de fluconazol por vía oral también fue similar en un estudio prospectivo y aleatorizado que incluyó a pacientes no neutropénicos y neutropénicos con candidiasis invasiva documentada o presunta. Sin embargo, hacen falta más estudios para evaluar mejor la eficacia relativa de la anfotericina B y del fluconazol en pacientes inmunodeprimidos o con infecciones graves.
Se recomienda fluconazol oral o anfotericina B IV cuando está indicado tratar la candiduria, por ejemplo en pacientes sintomáticos o neutropénicos, recién nacidos de bajo peso, pacientes con trasplante renal o pacientes sometidos a procedimientos urológicos; se prefiere fluconazol salvo que la infección esté causada por C. krusei o C. glabrata. También se ha utilizado la irrigación vesical con anfotericina B convencional. En un estudio aleatorizado en pacientes geriátricos hospitalizados con funguria causada por C. albicans, C. tropicalis o C. glabrata, 5 días de irrigación vesical con anfotericina B convencional (25 mg en 500 mL de solución de dextrosa al 5 % administrados mediante catéter vesical a una velocidad de 42 mL/hora) o un tratamiento de 5 días con fluconazol oral (dosis de carga de 200 mg el día 1 seguida de 100 mg una vez al día durante 4 días adicionales) erradicaron la funguria en el 83 o el 66 % de los pacientes, respectivamente.
El fluconazol también se usa como profilaxis para reducir la incidencia de candidiasis en receptores de trasplante de médula ósea que reciben quimioterapia o radioterapia. También se ha utilizado como profilaxis primaria frente a infecciones fúngicas, incluida la candidiasis, en un número limitado de pacientes considerados de alto riesgo para desarrollar estas infecciones, como pacientes oncológicos neutropénicos colonizados por Candida y/o tratados con corticosteroides, y determinados pacientes con SIDA.
El fluconazol se ha utilizado con buenos resultados en varios pacientes con endoftalmitis causada por Candida. Sin embargo, se han descrito fracasos terapéuticos y el papel del medicamento en el tratamiento de esta infección todavía no está claro. Estudios en conejos indican que el fluconazol se distribuye en el ojo y que inhibe el crecimiento de C. albicans en el tejido coroideo-retiniano y en el humor vítreo cuando el tratamiento IV se inicia en las 24 horas posteriores a la inoculación; no inhibió eficazmente el crecimiento del microorganismo cuando el tratamiento IV se inició 7 días después de la inoculación, cuando la infección ya estaba bien establecida.
Infecciones criptocócicas
El fluconazol por vía oral o intravenosa se utiliza en adultos inmunocompetentes o inmunodeprimidos para tratar la meningitis causada por C. neoformans. El medicamento ha sido eficaz como tratamiento inicial (primario) de la meningitis criptocócica aguda tanto en adultos con infección por VIH como en personas sin VIH. Ha logrado la resolución clínica de los signos y síntomas de la infección en aproximadamente el 34-75 % de estos pacientes. Aunque la anfotericina B (con o sin flucitosina) se considera el tratamiento inicial de elección para la meningitis criptocócica, el fluconazol es una alternativa en pacientes cuya enfermedad no es grave, ya que por lo general se tolera bien y alcanza concentraciones elevadas en el LCR. Aunque la experiencia en niños es limitada, el fluconazol también puede considerarse como alternativa a la terapia con anfotericina B en este grupo de edad.
El fluconazol ha sido eficaz en el tratamiento de la meningitis criptocócica aguda en algunos pacientes que no respondieron a la terapia con anfotericina B. Sin embargo, hay pruebas de que el fluconazol puede ser menos eficaz que la anfotericina B durante el tratamiento inicial de la meningitis criptocócica aguda en pacientes con SIDA y que puede tardar más en esterilizar el LCR. En un estudio multicéntrico aleatorizado que comparó anfotericina B (dosis media de 0,4-0,5 mg/kg/día durante 10 semanas con o sin flucitosina) con fluconazol oral (400 mg el primer día y después 200-400 mg durante 10 semanas) en pacientes con SIDA y meningitis criptocócica, el tratamiento fue eficaz en el 40 % de los pacientes que recibieron anfotericina B y en el 34 % de los que recibieron fluconazol. Aunque la mortalidad global fue similar entre ambos grupos (14 % con anfotericina B frente a 18 % con fluconazol), la mortalidad fue mayor durante las primeras 2 semanas de tratamiento en los pacientes que recibieron fluconazol (15 % frente a 8 % con anfotericina B). Los cultivos de LCR siguieron siendo positivos durante una media de aproximadamente 42 o 64 días en los pacientes tratados con anfotericina B o fluconazol, respectivamente. En otro estudio que comparó anfotericina B (0,7 mg/kg/día durante 1 semana, seguida de esta dosis 3 veces por semana durante 9 semanas combinada con flucitosina 150 mg/kg/día) con fluconazol oral (400 mg/día durante 10 semanas) en un número limitado de pacientes con SIDA y meningitis criptocócica, la terapia inicial fue eficaz en todos los pacientes que recibieron anfotericina B, pero solo en el 43 % de los que recibieron fluconazol; los cultivos de LCR fueron positivos durante una media aproximada de 16 y 41 días en los pacientes que recibieron estas terapias, respectivamente. Aunque los grupos de pacientes de este estudio eran similares en cuanto a la gravedad de la infección criptocócica, el recuento de células T cooperadoras/inductoras (CD4+, T4+) fue menor en el grupo de fluconazol, lo que dificulta la interpretación.
Muchos clínicos recomiendan que el tratamiento de la meningitis criptocócica en pacientes con infección por VIH se inicie con un régimen de anfotericina B intravenosa (con flucitosina) administrado durante al menos 2 semanas, o hasta que el paciente se estabilice, seguido de un régimen de fluconazol oral o itraconazol oral durante al menos 8-10 semanas más, o incluso más tiempo. Mientras se dispone de más datos y experiencia, algunos clínicos consideran que lo más prudente puede ser empezar con anfotericina B intravenosa (con o sin flucitosina) y continuar después con tratamiento de mantenimiento con fluconazol, al menos en pacientes con enfermedad más grave y en aquellos con mayor riesgo. En este contexto, el tratamiento primario con fluconazol probablemente debería reservarse para pacientes que no respondan adecuadamente a la anfotericina B o no la toleren, y para aquellos con enfermedad menos grave (por ejemplo, sin manifestaciones neurológicas y con títulos bajos de antígeno criptocócico en LCR).
La eficacia relativa del tratamiento inicial con anfotericina B convencional por vía intravenosa (0,7 mg/kg/día), administrada junto con flucitosina (100 mg/kg/día) o placebo durante 2 semanas, seguida de fluconazol por vía oral (800 mg/día durante 2 días y después 400 mg/día durante 8 semanas) o itraconazol por vía oral (600 mg/día durante 3 días y después 400 mg/día durante 8 semanas), se ha evaluado en un ensayo multicéntrico doble ciego en pacientes con meningitis criptocócica asociada al sida. A las 2 semanas, los cultivos de LCR fueron negativos en el 60 % de los pacientes que recibieron anfotericina B con flucitosina, frente al 51 % de los que recibieron anfotericina B sola. La respuesta clínica al fluconazol por vía oral o al itraconazol por vía oral como tratamiento de continuación fue similar, pero la tasa de esterilización del LCR a las 10 semanas fue mayor en quienes recibieron fluconazol (72 %) que en quienes recibieron itraconazol (60 %).
Se ha utilizado un régimen de fluconazol oral (400 mg/día para infecciones pulmonares o 400-800 mg/día para infecciones del SNC) y flucitosina oral (100-150 mg/kg/día) como alternativa para el tratamiento de infecciones criptocócicas pulmonares o del SNC en un número limitado de pacientes. Aunque el fluconazol junto con flucitosina puede ser eficaz para tratar infecciones criptocócicas pulmonares leves o moderadas, este régimen ha sido ineficaz en algunos pacientes con meningitis criptocócica. No se recomienda como tratamiento inicial de estas infecciones. Además, cuando se usa para tratar la meningitis criptocócica en personas con infección por VIH, el régimen de fluconazol y flucitosina se ha asociado con una alta incidencia de efectos secundarios, lo que ha llevado a suspender la flucitosina en el 28 % de los pacientes.
La tasa de mortalidad en pacientes con SIDA durante el primer episodio de meningitis criptocócica ha sido aproximadamente del 25-58 % a pesar del tratamiento con anfotericina B. En pacientes con SIDA que responden al tratamiento antifúngico inicial, la tasa de recaída de la infección criptocócica es del 35-65 %. La terapia antifúngica de mantenimiento o supresora crónica suele considerarse necesaria después del tratamiento inicial de la infección, salvo que se haya producido una recuperación inmunitaria gracias a una terapia antirretroviral potente.
El fluconazol oral ha sido eficaz cuando se usa como terapia de mantenimiento a largo plazo para prevenir recaídas de la meningitis criptocócica en pacientes con SIDA. Los resultados de un estudio multicéntrico que comparó la seguridad y eficacia del fluconazol oral (200 mg una vez al día) con anfotericina B IV (1 mg/kg una vez a la semana) para prevenir recaídas en pacientes con SIDA que tenían cultivos criptocócicos negativos tras un tratamiento inicial adecuado con anfotericina B indican que el régimen con fluconazol es más eficaz, en términos de prevención de recaídas de meningitis con cultivo positivo, y se tolera mejor que el régimen con anfotericina B como tratamiento de mantenimiento en estos pacientes. En un estudio multicéntrico que comparó el mantenimiento con fluconazol oral (100-200 mg/día) frente a placebo en estos pacientes, el riesgo acumulado global estimado de recurrencia criptocócica en cualquier localización tras 1 año de mantenimiento con fluconazol fue del 5 % frente al 100 % con placebo.
La eficacia del mantenimiento con fluconazol para prevenir la recaída criptocócica en pacientes con infección prostática persistente tras la terapia antifúngica inicial parece ser menor que en la población general. Sin embargo, esta menor eficacia puede superarse al menos en parte aumentando la dosis del medicamento. En un número limitado de adultos con SIDA que presentaban criptococosis urinaria persistente, incluidas infecciones prostáticas, tras un tratamiento inicial adecuado con anfotericina B (con o sin flucitosina) para meningitis criptocócica, la terapia de mantenimiento con fluconazol oral produjo curación micológica en la mayoría de los pacientes. Por el contrario, en los pacientes restantes se produjo recaída de la criptococosis (con masaje prostático) y/o infección sistémica durante el mantenimiento con fluconazol.
La respuesta en estos pacientes -supresión mantenida del criptococo inducido por masaje prostático y ausencia de signos de recaída sistémica o del SNC- parece depender de la dosis y por lo general requiere dosis orales de fluconazol de 200-600 mg al día. Además, pueden hacer falta varias semanas o meses de mantenimiento con fluconazol para que esa respuesta se manifieste. En un estudio, se estimó que la probabilidad de respuesta era del 36 % tras 4 semanas y del 59 % tras 27 semanas de mantenimiento. Dosis relativamente altas (por ejemplo, 600 mg al día o más) pueden esterilizar de forma eficaz múltiples abscesos prostáticos grandes en algunos pacientes. Aun así, todavía no están claros los factores que pueden predecir la respuesta ni cuál es la terapia antifúngica óptima en estos pacientes. Además, debido al riesgo de recaída, algunos clínicos advierten de que debe descartarse bien la posibilidad de un foco prostático de infección en cualquier paciente varón si se plantea un mantenimiento con fluconazol a dosis bajas.
El fluconazol oral ha sido eficaz en un número limitado de pacientes para tratar la criptococosis cutánea o subcutánea. El medicamento también ha sido eficaz para tratar la neumonía criptocócica en un número limitado de pacientes, aunque en algunos fue necesaria la extirpación quirúrgica del foco de infección; aun así, debe tenerse en cuenta la posibilidad de que la neumonía criptocócica sea una manifestación de una infección diseminada.
Coccidioidomicosis
El fluconazol oral se ha usado con éxito en el tratamiento de la coccidioidomicosis causada por Coccidioides immitis (por ejemplo, meningitis, infecciones pulmonares e infecciones diseminadas, incluidas las de tejidos blandos o huesos y articulaciones). En adultos con meningitis coccidioidal, el fluconazol ha mostrado mejoría clínica y/o analítica cuando se ha utilizado solo o junto con anfotericina B. El fluconazol oral se ha usado para tratar la meningitis coccidioidal tanto en personas con infección por VIH como en seronegativas. Como el fluconazol suele tolerarse bien y presenta una farmacocinética favorable (por ejemplo, alcanza concentraciones altas en el LCR tras la administración oral o IV), se considera una alternativa menos tóxica a la anfotericina B para el tratamiento de la meningitis coccidioidal y otras infecciones coccidioidales persistentes, especialmente porque estas infecciones suelen requerir tratamiento antifúngico prolongado. El fluconazol se considera un medicamento de elección para tratar la coccidioidomicosis; sin embargo, la anfotericina B IV suele preferirse como tratamiento inicial de la coccidioidomicosis grave, sobre todo en pacientes inmunodeprimidos, incluidos los que tienen infección por VIH. Se necesitan más estudios para evaluar la eficacia y establecer la dosis oral óptima de fluconazol para la coccidioidomicosis, así como para determinar si el medicamento reduce de forma sustancial la morbilidad y la mortalidad. Algunos datos indican que la tasa de respuesta puede mejorar cuando se usan dosis más altas de fluconazol (es decir, 400 mg al día o más). También se ha sugerido que el uso de dosis relativamente bajas (por ejemplo, 50-100 mg al día) puede contribuir al riesgo de recurrencia de la infección.
Blastomicosis
El fluconazol oral se ha utilizado para tratar la blastomicosis causada por Blastomyces dermatitidis, aunque esta infección es poco frecuente en España. Mientras que el itraconazol oral o la anfotericina B IV se consideran medicamentos de elección para el tratamiento de la blastomicosis, el fluconazol oral o el ketoconazol oral se consideran alternativas. La anfotericina B IV suele preferirse para tratar infecciones graves, especialmente las que afectan al SNC, y como tratamiento inicial de la blastomicosis presunta en pacientes inmunodeprimidos, incluidos los que tienen infección por VIH.
Hay pruebas de que el itraconazol oral puede ser más eficaz que el fluconazol oral o el ketoconazol oral para tratar la blastomicosis. Muchos clínicos consideran que el itraconazol es el antifúngico azólico de elección para la blastomicosis no meníngea y no potencialmente mortal, y también lo recomiendan como tratamiento de continuación en pacientes con infecciones más graves tras una respuesta inicial con anfotericina B IV. Al elegir un antifúngico para pacientes con blastomicosis, debe tenerse en cuenta que se han descrito fracasos terapéuticos cuando se utilizó un antifúngico oral (por ejemplo, ketoconazol) para tratar blastomicosis cutánea o pulmonar en pacientes que ya tenían afectación asintomática o subclínica del SNC en el momento del diagnóstico inicial.
Histoplasmosis
El fluconazol oral se ha usado con cierto éxito para tratar la histoplasmosis causada por Histoplasma capsulatum. Mientras que la anfotericina B IV o el itraconazol oral se consideran medicamentos de elección para el tratamiento de la histoplasmosis, el fluconazol oral o el ketoconazol oral se consideran alternativas. El fluconazol oral (400-800 mg/día) ha sido eficaz en un número limitado de pacientes con infección por VIH y con histoplasmosis diseminada leve o moderadamente grave; sin embargo, la anfotericina B IV suele preferirse para el tratamiento inicial de la histoplasmosis grave y potencialmente mortal, especialmente en pacientes inmunodeprimidos, como aquellos con infección por VIH. Además, el itraconazol oral suele ser el antifúngico azólico preferido para tratar la histoplasmosis leve o moderada, o como tratamiento de continuación de infecciones graves tras una respuesta con anfotericina B.
Esporotricosis
El fluconazol se utiliza como alternativa para el tratamiento de la esporotricosis. La anfotericina B IV suele considerarse el medicamento de elección para el tratamiento inicial de infecciones graves y potencialmente mortales, y siempre que haya afectación del SNC. El itraconazol oral se considera el medicamento de elección para tratar la esporotricosis cutánea, linfocutánea, pulmonar u osteoarticular leve, y para el tratamiento de continuación en infecciones más graves tras obtenerse una respuesta con anfotericina B IV. El fluconazol se considera una terapia de segunda línea para la esporotricosis cutánea, linfocutánea u osteoarticular y, como puede ser menos eficaz que el itraconazol, solo debe usarse si el paciente no puede tolerar el itraconazol. Algunos clínicos afirman que el fluconazol no es eficaz y que no debe usarse para tratar la esporotricosis pulmonar.
Aspergilosis
El fluconazol se ha usado por vía oral, intravenosa o mediante infusión intracavitaria en algunos adultos para tratar la neumonía u otras infecciones del tracto respiratorio causadas por Aspergillus fumigatus, A. niger o A. terreus. En un estudio, el fluconazol mostró una eficacia clínica del 23-53 % en infecciones por Aspergillus y una tasa de curación micológica de aproximadamente el 50 % en infecciones por A. fumigatus. El fluconazol ha mostrado resultados variables en el tratamiento de infecciones causadas por Aspergillus. La anfotericina B IV se considera generalmente el medicamento de elección, y el itraconazol suele ser la alternativa preferida para tratar la aspergilosis.
Dermatofitosis
El fluconazol oral ha sido eficaz en el tratamiento de ciertas dermatofitosis (por ejemplo, tiña capitis, tiña corporis, tiña cruris y tiña pedis) causadas por Epidermophyton, Microsporum o Trichophyton. El fluconazol oral también ha sido eficaz para tratar la pitiriasis versicolor y la onicomicosis.
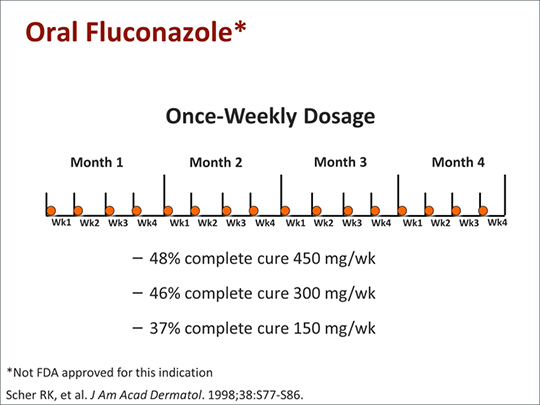
El fluconazol oral (3-6 mg/kg/día durante 2-6 semanas) ha tratado con eficacia la tiña capitis en niños de 1,5 a 16 años y ha logrado curación clínica y micológica en aproximadamente el 88-90 % de los pacientes. Para el tratamiento de la tiña corporis, la tiña cruris o la tiña pedis en adultos, el fluconazol oral ha sido eficaz en un régimen semanal (150 mg una vez por semana durante 2-6 semanas). Hay pruebas de que este régimen semanal es tan eficaz como un régimen diario de fluconazol (50 mg una vez al día) para tratar estas infecciones. Los resultados de un estudio aleatorizado indican que la tasa de erradicación al final del tratamiento en pacientes con tiña corporis o tiña cruris es del 82-88 % en quienes reciben el régimen semanal y del 94-100 % en quienes reciben el régimen diario; en el seguimiento al mes, las tasas globales de erradicación fueron del 91-100 % y del 91-94 %, respectivamente. Aunque no se ha identificado el régimen óptimo de dosificación de fluconazol oral para tratar la onicomicosis, un régimen oral semanal de fluconazol (150-450 mg una vez a la semana durante 3-12 meses) ha sido eficaz para el tratamiento de la onicomicosis de las uñas de los pies en un número limitado de adultos. Sin embargo, se necesitan más estudios, y hay indicios de que el fluconazol podría ser menos eficaz que el itraconazol oral o la terbinafina oral para tratar la onicomicosis.
La tiña corporis y la tiña cruris suelen poder tratarse eficazmente con un antifúngico tópico; sin embargo, puede ser necesario un tratamiento antifúngico oral si la enfermedad es extensa, hay foliculitis por dermatofitos, la infección es crónica o no responde al tratamiento tópico, o si el paciente está inmunodeprimido o tiene otras enfermedades. La tiña capitis y la tiña barbae suelen tratarse con un antifúngico oral. Aunque los antifúngicos tópicos suelen ser adecuados para tratar la tiña manuum y la tiña pedis no complicadas, a menudo son necesarios tratamientos antifúngicos orales para las zonas hiperqueratósicas de palmas y plantas, para la tiña pedis crónica tipo mocasín (tipo seco) y para la tiña unguium (onicomicosis).
Prevención de infecciones fúngicas en personas con infección por VIH
El fluconazol se ha utilizado en personas con infección por VIH para la profilaxis primaria frente a infecciones fúngicas graves (por ejemplo, criptococosis) y como terapia supresora a largo plazo o de mantenimiento crónico (profilaxis secundaria) para prevenir la recurrencia o recaída de ciertas infecciones fúngicas (por ejemplo, coccidioidomicosis, criptococosis y candidiasis mucocutánea).
En España, las recomendaciones sobre la prevención de infecciones oportunistas, incluidas las infecciones fúngicas, en personas con VIH suelen seguir la práctica nacional junto con las guías de expertos europeas, e incluyen consejos para reducir la exposición a patógenos oportunistas, prevenir los episodios iniciales de enfermedad y evitar las recaídas. La guía actual no recomienda la profilaxis primaria para prevenir los primeros episodios de candidiasis mucocutánea en adultos, adolescentes, lactantes y niños con infección por VIH. Asimismo, la profilaxis primaria rutinaria para prevenir los primeros episodios de coccidioidomicosis, criptococosis o histoplasmosis en adultos, adolescentes, lactantes y niños con infección por VIH no suele recomendarse, aunque la profilaxis frente a criptococosis o histoplasmosis puede considerarse en personas seleccionadas. Los adultos, adolescentes, lactantes y niños con infección por VIH que hayan completado el tratamiento inicial de una coccidioidomicosis, criptococosis o histoplasmosis documentada pueden necesitar terapia supresora a largo plazo o tratamiento de mantenimiento (profilaxis secundaria) para prevenir la recurrencia o recaída de estas infecciones fúngicas. Además, las personas con infección por VIH que presentan recurrencias frecuentes o graves de candidiasis mucocutánea (orofaríngea, esofágica o vaginal) pueden beneficiarse de una terapia supresora a largo plazo o de mantenimiento.
Debido a las preocupaciones sobre el uso de antifúngicos azólicos orales durante el embarazo, no debe usarse fluconazol para profilaxis primaria ni como terapia supresora o de mantenimiento crónico en mujeres embarazadas. Si una mujer se queda embarazada mientras recibe profilaxis con fluconazol y decide continuar con el embarazo, debe suspender la profilaxis. Se recomiendan métodos anticonceptivos eficaces para todas las mujeres con infección por VIH que reciban un antifúngico azólico oral como terapia supresora. La anfotericina B intravenosa convencional puede ser el agente preferido si se necesita terapia supresora o tratamiento de mantenimiento a largo plazo frente a coccidioidomicosis, criptococosis o histoplasmosis en una mujer embarazada con infección por VIH, especialmente durante el primer trimestre.
Profilaxis primaria
Coccidioidomicosis
La guía actual indica que no se recomienda la profilaxis primaria rutinaria frente a la coccidioidomicosis en pacientes con infección por VIH que viven en zonas endémicas. Algunos clínicos sugieren que debe considerarse la profilaxis primaria en personas con infección por VIH que tienen una prueba serológica CF positiva sin enfermedad activa. Sin embargo, no está claro si la profilaxis primaria sería útil en personas con infección por VIH que viven en áreas endémicas de coccidioidomicosis. Se ha desarrollado coccidioidomicosis activa en personas con infección por VIH que recibían terapia con azólicos para otras afecciones. La prueba cutánea rutinaria para coccidioidomicosis en personas con infección por VIH que viven en zonas endémicas no predice la enfermedad y, por lo general, no se recomienda. Dentro de una zona endémica, una serología positiva podría indicar un mayor riesgo de infección activa; sin embargo, las pruebas serológicas rutinarias no parecen útiles y no suelen recomendarse.
Criptococosis
La guía actual indica que, aunque no se recomienda la profilaxis primaria rutinaria frente a la criptococosis, puede considerarse en adultos y adolescentes con VIH con recuentos de células T CD4+ inferiores a 50/mm3, así como en lactantes y niños con inmunosupresión grave (según los criterios ajustados por edad). No se recomienda de forma rutinaria debido a la frecuencia relativamente baja de la enfermedad criptocócica, a la falta de pruebas de un beneficio en la supervivencia y a la preocupación por las interacciones farmacológicas, el posible desarrollo de resistencias y el coste. Al decidir sobre la profilaxis primaria frente a la criptococosis, también debe valorarse la necesidad de profilaxis primaria o tratamiento supresor frente a otras infecciones fúngicas, como la coccidioidomicosis, la histoplasmosis o la candidiasis mucocutánea. Tampoco se recomienda realizar de forma rutinaria pruebas de antígeno criptocócico sérico en personas asintomáticas, ya que es poco probable que los resultados cambien las decisiones clínicas. Las personas con VIH no pueden evitar por completo la exposición a Cryptococcus neoformans; no hay pruebas de que la exposición a excrementos de paloma se asocie con un mayor riesgo de criptococosis.
El fluconazol por vía oral es el tratamiento de elección para la profilaxis primaria frente a la criptococosis en adultos, adolescentes, lactantes y niños con VIH, e itraconazol por vía oral en cápsulas se considera una alternativa.
Histoplasmosis
La guía actual indica que puede considerarse la profilaxis primaria frente a la histoplasmosis en adultos o adolescentes con VIH con recuentos de células T CD4+ inferiores a 100/mm3 que tengan un alto riesgo, especialmente por exposición laboral a Histoplasma capsulatum o por vivir en una comunidad con una tasa hiperendémica de histoplasmosis (al menos 10 casos/100 años-paciente). También puede valorarse en lactantes o niños con VIH e inmunosupresión grave que vivan en zonas endémicas de histoplasmosis. Al decidir si usar profilaxis primaria frente a la histoplasmosis en estas personas, los profesionales sanitarios deben tener en cuenta la incidencia local de la enfermedad, la posibilidad de interacciones farmacológicas, la toxicidad, el desarrollo de resistencias, el coste y la necesidad de profilaxis frente a otras infecciones fúngicas, como la candidiasis o la criptococosis.
El tratamiento de primera elección para la profilaxis primaria frente a la histoplasmosis en adultos, adolescentes o pacientes pediátricos con VIH es itraconazol por vía oral en cápsulas; la guía actual no hace recomendaciones sobre una alternativa a itraconazol. Hay algunas pruebas de que el fluconazol por vía oral puede no ser eficaz para prevenir los primeros episodios de histoplasmosis.
Candidiasis mucocutánea
La guía actual indica que no se recomienda la profilaxis primaria para prevenir los primeros episodios de candidiasis mucocutánea (esofágica, orofaríngea o vaginal) en adultos, adolescentes, lactantes o niños con VIH, ya que la candidiasis mucocutánea aguda suele poder tratarse y rara vez pone en peligro la vida. También influye la preocupación por el posible desarrollo de Candida resistente, las posibles interacciones farmacológicas y el coste de la profilaxis antifúngica.
Prevención de la recurrencia
Coccidioidomicosis
La guía actual recomienda que las personas con VIH que hayan completado el tratamiento inicial de una coccidioidomicosis documentada reciban tratamiento supresor o de mantenimiento a largo plazo (profilaxis secundaria) para prevenir la recurrencia o la recaída. El fluconazol por vía oral se considera, por lo general, el tratamiento de elección, y la anfotericina B IV e itraconazol por vía oral en cápsulas son alternativas. El tratamiento supresor a largo plazo para prevenir la recurrencia o la recaída de la coccidioidomicosis en adultos, adolescentes, lactantes y niños con VIH suele mantenerse de por vida. Aunque las personas con VIH pueden tener un riesgo bajo de recurrencia de infecciones fúngicas sistémicas si su recuento de células T CD4+ aumenta por encima de 100/mm3 mientras reciben tratamiento antirretroviral combinado potente, los datos disponibles siguen siendo insuficientes para respaldar una recomendación firme sobre la interrupción de la profilaxis frente a la coccidioidomicosis en estos pacientes.
Criptococosis
La guía actual recomienda que las personas con VIH que hayan completado el tratamiento inicial de una criptococosis documentada reciban tratamiento supresor o de mantenimiento a largo plazo (profilaxis secundaria) para prevenir la recurrencia o la recaída, salvo que se haya producido una recuperación inmunitaria como resultado de un tratamiento antirretroviral combinado potente. El fluconazol por vía oral se considera, por lo general, el tratamiento de elección, y la anfotericina B IV e itraconazol por vía oral en cápsulas son alternativas. Un estudio aleatorizado, doble ciego y controlado en personas con VIH con meningitis criptocócica documentada y tratada adecuadamente aporta algunas pruebas de que el fluconazol por vía oral (200 mg una vez al día) es más eficaz que el itraconazol por vía oral (200 mg una vez al día) como tratamiento supresor en estos pacientes, ya que la tasa de recaída de criptococosis con cultivo positivo fue del 4 % en quienes recibieron fluconazol, frente al 23 % en quienes recibieron itraconazol.

El tratamiento supresor o de mantenimiento para prevenir la recurrencia o la recaída de la criptococosis en personas con VIH suele mantenerse de por vida, salvo que se haya producido una recuperación inmunitaria como resultado de un tratamiento antirretroviral combinado potente. Los datos limitados indican que interrumpir el tratamiento supresor o de mantenimiento en adultos y adolescentes con VIH que hayan completado el tratamiento inicial de la criptococosis, permanezcan asintomáticos respecto a esta infección y presenten aumentos sostenidos (por ejemplo, durante 6 meses o más) del recuento de células T CD4+ por encima de 100-200/mm3 en respuesta al tratamiento antirretroviral potente se asocia con un bajo riesgo de recurrencia. Con base en ello y en datos más amplios sobre la seguridad de suspender el tratamiento supresor a largo plazo en otras infecciones oportunistas, es razonable considerar la interrupción de la terapia supresora en las personas que cumplan estos criterios. Puede haber recurrencias en quienes interrumpan el tratamiento supresor, y este debe reiniciarse si el recuento de células T CD4+ desciende por debajo de 100-200/mm3. No se ha estudiado la seguridad de interrumpir el tratamiento supresor en lactantes y niños con VIH, y los niños deben recibir tratamiento supresor de por vida después de un episodio de criptococosis.
Histoplasmosis
Para el tratamiento supresor a largo plazo en pacientes con VIH con histoplasmosis documentada y tratada adecuadamente, itraconazol por vía oral en cápsulas se considera, por lo general, el tratamiento de elección, y la anfotericina B IV, una alternativa.
Candidiasis mucocutánea
Debe valorarse el uso de tratamiento supresor o de mantenimiento a largo plazo en adultos y adolescentes con antecedentes de candidiasis esofágica documentada, especialmente si han tenido múltiples episodios, teniendo en cuenta el posible desarrollo de cepas resistentes de Candida. Además, debe considerarse el tratamiento supresor en lactantes y niños con candidiasis mucocutánea grave y recurrente, especialmente si presentan candidiasis esofágica. Aunque muchos expertos no recomiendan la profilaxis a largo plazo frente a la candidiasis recurrente orofaríngea o vulvovaginal en pacientes con VIH por las mismas razones por las que no recomiendan la profilaxis primaria rutinaria frente a la candidiasis, puede valorarse el tratamiento supresor en personas con VIH que presentan recurrencias frecuentes o graves de estas infecciones candidiásicas. Al considerar este tratamiento, deben tenerse en cuenta varios factores, como el impacto de las recurrencias en el bienestar y la calidad de vida del paciente, la necesidad de profilaxis frente a otras infecciones fúngicas, el coste de la profilaxis, la toxicidad de los medicamentos, las interacciones farmacológicas y el posible desarrollo de resistencias a los fármacos entre Candida y otros hongos.
Si está indicado un tratamiento supresor a largo plazo como profilaxis frente a la candidiasis mucocutánea en adultos, adolescentes, lactantes o niños con VIH con recurrencias frecuentes o graves de candidiasis orofaríngea, esofágica o vaginal, generalmente se recomienda fluconazol por vía oral como tratamiento de elección, e itraconazol en solución oral como alternativa.
El tratamiento supresor a largo plazo para prevenir la recurrencia o la recaída de infecciones fúngicas en pacientes con VIH suele mantenerse de por vida. En algunos pacientes con VIH que habían recibido fluconazol por vía oral para prevenir la recurrencia de candidiasis orofaríngea durante una duración media de 18 meses (intervalo: 4-98 meses) y que estaban en tratamiento antirretroviral combinado potente (alrededor del 50 % tenían niveles plasmáticos de ARN VIH-1 por debajo de los límites de detección), la interrupción del tratamiento supresor con fluconazol oral dio lugar a una recurrencia de candidiasis orofaríngea en solo el 10 % de los pacientes dentro de los 6-11 meses. Aunque los pacientes con VIH que reciben profilaxis antifúngica supresora pueden tener un bajo riesgo de recurrencia de infecciones fúngicas si sus recuentos de células T CD4+ aumentan por encima de 100/mm3 mientras reciben tratamiento antirretroviral combinado potente, los datos disponibles siguen siendo insuficientes para respaldar una recomendación firme sobre la interrupción de la profilaxis en estos pacientes.
Prevención de infecciones fúngicas en pacientes trasplantados y con cáncer
El fluconazol se utiliza de forma profiláctica para reducir la incidencia de candidiasis en pacientes sometidos a trasplante de médula ósea (BMT) que reciben quimioterapia o radioterapia. El fármaco también se ha utilizado para la profilaxis de infecciones fúngicas en pacientes sometidos a trasplante hepático y en pacientes con cáncer considerados en riesgo de neutropenia e infecciones fúngicas. Hay algunas pruebas de que la profilaxis con fluconazol en pacientes trasplantados y con cáncer puede reducir la frecuencia de candidiasis orofaríngea y/o sistémica durante el periodo previo a la recuperación de neutrófilos. Además, la profilaxis con fluconazol puede reducir la necesidad de tratamiento antifúngico empírico en estos pacientes. La eficacia del fluconazol por vía oral (400 mg una vez al día) para la profilaxis de infecciones fúngicas en pacientes neutropénicos se evaluó en un estudio aleatorizado y controlado con placebo en el que participaron 274 pacientes con cáncer de 18-80 años que recibían quimioterapia citotóxica o tratamiento de acondicionamiento para BMT. Aunque el porcentaje de pacientes que no necesitaron tratamiento empírico con anfotericina B IV fue similar en ambos grupos (el 57 % de los que recibieron fluconazol y el 50 % de los que recibieron placebo no lo necesitaron), el éxito completo sin colonización fúngica se alcanzó en el 37 % de los que recibieron fluconazol y en el 20 % de los que recibieron placebo. Además, la incidencia de infecciones fúngicas superficiales fue menor en quienes recibieron fluconazol (7 %) que en quienes recibieron placebo (18 %), y solo el 3 % de los tratados con fluconazol desarrolló infecciones fúngicas invasivas definidas, frente al 17 % de los que recibieron placebo. Aunque la profilaxis con fluconazol no afectó a la tasa global de mortalidad, el análisis por intención de tratar indica que el número de muertes atribuidas a infecciones fúngicas invasivas definidas fue menor en el grupo de fluconazol (1 de 15) que en el grupo placebo (6 de 15).
El uso de profilaxis antifúngica primaria en pacientes con cáncer sometidos a tratamiento mielosupresor o en pacientes sometidos a BMT o a trasplante de órganos sólidos sigue siendo controvertido, especialmente porque esta profilaxis puede favorecer la colonización por hongos resistentes y/o dar lugar a la aparición de microorganismos muy resistentes. Los estudios retrospectivos han mostrado un aumento del riesgo de colonización por Candida krusei en receptores de BMT y en pacientes neutropénicos que recibieron profilaxis con fluconazol; en un estudio, aproximadamente el 41 % de los pacientes que recibieron fluconazol presentaban colonización por C. krusei, frente al 17 % de los que no lo recibieron. Por ello, la mayoría de los profesionales sanitarios suelen desaconsejar la profilaxis antifúngica primaria, salvo en determinados pacientes de alto riesgo cuidadosamente seleccionados en los que se espera que los beneficios potenciales compensen los posibles riesgos. Aun así, muchos expertos señalan que deberían continuar los estudios controlados y aleatorizados para evaluar el uso de fluconazol en la prevención de infecciones fúngicas en pacientes con cáncer y en receptores de BMT.
Dosificación y administración
El fluconazol es un antifúngico triazólico que se usa para la candidiasis mucosa superficial (orofaríngea, esofágica o vaginal) y para infecciones fúngicas cutáneas. También se administra para infecciones sistémicas, como la candidiasis sistémica, la coccidioidomicosis y la criptococosis. Se ha estudiado en blastomicosis, histoplasmosis y esporotricosis.
El fluconazol se administra por vía oral o intravenosa en dosis similares. En perfusión intravenosa, se administra como una solución de 2 mg/mL a una velocidad de 5 a 10 mL/minuto (300 a 600 mL/hora). En la práctica, la velocidad de perfusión debe seguir la información autorizada del producto utilizada en España.
Para la candidiasis mucosa superficial (excepto la candidiasis genital), la dosis habitual de fluconazol por vía oral en España es de 50 mg al día. No obstante, si es necesario, puede administrarse 100 mg al día.
El tratamiento suele mantenerse entre 7 y 14 días en la candidiasis orofaríngea (excepto en pacientes gravemente inmunodeprimidos), durante 14 días en la candidiasis oral atrófica asociada a prótesis dental, y entre 14 y 30 días en otras infecciones candidiásicas de las mucosas, incluida la esofagitis. En EE. UU. se recomiendan dosis más altas: una dosis inicial de 200 mg de fluconazol seguida de 100 mg al día, con un tratamiento mínimo de 14 días para la infección orofaríngea, o de al menos 21 días y al menos 14 días después de la desaparición de los síntomas para las infecciones esofágicas; si es necesario, pueden utilizarse dosis de hasta 400 mg al día para la candidiasis esofágica.
Administración oral
El fluconazol puede administrarse por vía oral con o sin alimentos. El polvo para suspensión oral de fluconazol debe reconstituirse en el momento de la dispensación añadiendo 24 mL de agua destilada o purificada al envase que contiene 0,35 o 1,4 g del fármaco, para obtener una suspensión con 50 o 200 mg/5 mL, respectivamente. El frasco debe agitarse enérgicamente para suspender el polvo, y la suspensión debe volver a agitarse bien justo antes de administrarla.
Administración IV
Las perfusiones intravenosas de fluconazol deben administrarse una vez al día a una velocidad que no exceda los 200 mg/hora. Las soluciones inyectables de fluconazol para perfusión intravenosa deben inspeccionarse visualmente antes de su administración para comprobar que no presenten decoloración ni partículas, siempre que la solución y el envase lo permitan. La solución para perfusión debe desecharse si está turbia o presenta precipitados, o si el cierre no está intacto. Los envases Viaflex® Plus de fluconazol deben comprobarse para detectar pequeñas fugas apretando firmemente la bolsa. La solución debe desecharse si el cierre del envase no está intacto, si se detectan fugas o si la solución está turbia o contiene precipitados. No deben añadirse aditivos al envase plástico de la solución inyectable. La solución inyectable en envases plásticos no debe usarse en conexiones en serie con otros envases plásticos, ya que esto podría provocar una embolia gaseosa por el aire residual aspirado del envase primario antes de que finalice la administración desde el envase secundario.
Puede utilizarse una dosis única de 150 mg de fluconazol por vía oral para la candidiasis genital (candidiasis vaginal o balanitis candidiásica). La dermatofitosis, la pitiriasis versicolor y las infecciones cutáneas por Candida pueden tratarse con fluconazol 50 mg por vía oral una vez al día durante un máximo de seis semanas.
La candidiasis sistémica, la meningitis criptocócica y otras infecciones criptocócicas pueden tratarse por vía oral o mediante perfusión intravenosa con fluconazol. La dosis inicial es de 400 mg, seguida de 200 a 400 mg al día. La duración del tratamiento depende de la respuesta clínica y micológica, pero por lo general es de al menos 6 a 8 semanas. En la meningitis criptocócica, el tratamiento suele mantenerse entre 10 y 12 semanas después de que los cultivos de LCR sean negativos.
El fluconazol también puede utilizarse en dosis diarias de 100 a 200 mg por vía oral o intravenosa para prevenir la recaída tras un tratamiento antifúngico inicial de la meningitis criptocócica aguda en pacientes con SIDA. En pacientes inmunodeprimidos con riesgo de infecciones fúngicas, el fluconazol puede administrarse de forma profiláctica por vía oral o en perfusión intravenosa en dosis de 50 a 400 mg al día. Sin embargo, la profilaxis a largo plazo se ha asociado con la aparición de microorganismos resistentes. En niños mayores de 4 semanas, las dosis son de 3 mg/kg/día para infecciones superficiales (puede utilizarse una dosis de carga de 6 mg/kg el primer día si es necesario) y de 6 a 12 mg/kg/día para infecciones sistémicas. En niños inmunodeprimidos, pueden administrarse dosis de 3 a 12 mg/kg/día como profilaxis. En lactantes menores de 2 semanas, todas estas dosis deben administrarse una vez cada 72 horas. En niños de entre 2 y 4 semanas, las dosis deben administrarse cada 48 horas.
No debe superarse una dosis máxima de 400 mg al día en niños ni de 12 mg/kg en los intervalos adecuados en lactantes. Puede ser necesario reducir la dosis en pacientes con insuficiencia renal.
Dosis elevadas
Se han estudiado dosis superiores a las recomendadas en la información autorizada del producto para fluconazol en pacientes con infecciones potencialmente mortales causadas por Candida spp., Cryptococcus neoformans y Coccidioides immitis.
Los estudios de determinación de dosis han encontrado que dosis diarias de 800 a 1000 mg de fluconazol son eficaces y bien toleradas. En un estudio con 11 pacientes con VIH que recibieron fluconazol 800 a 1000 mg al día por vía intravenosa durante 3 semanas, seguido de tratamiento por vía oral hasta que el cultivo de LCR se volvió negativo, 6 pacientes respondieron a las 10 semanas y otros 2 mejoraron clínicamente. Se han utilizado dosis diarias de hasta 800 mg en blastomicosis y coccidioidomicosis, y se han estudiado dosis de 10 mg/kg/día en candidiasis diseminada.
Dosis intermitentes
Existe preocupación por el uso cada vez más extendido del fluconazol, especialmente por el impacto del tratamiento continuo en pacientes inmunodeprimidos sobre el desarrollo de resistencias. Aun así, el fluconazol sigue utilizándose con frecuencia para la profilaxis primaria y secundaria. Algunos investigadores han sugerido pautas intermitentes, aunque esto podría aumentar aún más el riesgo de infecciones por microorganismos resistentes. Se ha estudiado el tratamiento semanal con fluconazol en la onicomicosis y la tiña capitis.
Administración en insuficiencia renal
Los pacientes con insuficiencia renal pueden necesitar una reducción de dosis. El primer día de tratamiento deben administrarse las dosis habituales de carga o iniciales de fluconazol, y las dosis posteriores deben ajustarse según el aclaramiento de creatinina (AC):
- AC superior a 50 mL/minuto: 100 % de la dosis estándar recomendada;
- AC inferior a 50 mL/minuto y sin diálisis: 50 % de la dosis estándar recomendada;
- pacientes en hemodiálisis regular: 100 % de la dosis estándar recomendada después de cada sesión de diálisis. No se requiere ajuste de dosis en pacientes con insuficiencia renal que reciben tratamiento en dosis única.
Dosificación en adultos
Candidiasis orofaríngea y esofágica
Para tratar la candidiasis orofaríngea o esofágica, la dosis habitual de fluconazol en adultos es de 200 mg como dosis única el primer día, seguida de 100 mg o 200 mg una vez al día. Según la respuesta del paciente, pueden usarse dosis de hasta 400 mg una vez al día. Aunque la candidiasis orofaríngea suele resolverse a los pocos días de empezar el tratamiento con fluconazol, el fabricante y algunos clínicos recomiendan mantenerlo al menos 2 semanas para reducir la probabilidad de recaída.

Sin embargo, otros clínicos cuestionan la necesidad de tratamientos prolongados en pacientes con esta infección. Los pacientes con candidiasis esofágica deben recibir tratamiento con fluconazol durante al menos 3 semanas y, además, durante al menos 2 semanas después de que desaparezcan los síntomas. No se ha establecido la dosis óptima para el tratamiento de mantenimiento en pacientes con candidiasis orofaríngea. En estos pacientes, se han utilizado habitualmente dosis orales de 50-100 mg una vez al día con buenos resultados; en ocasiones se han usado dosis de hasta 200 mg una vez al día.
Candidiasis vulvovaginal
Para tratar la candidiasis vulvovaginal no complicada en mujeres no embarazadas, la dosis habitual de fluconazol por vía oral es una dosis única de 150 mg. En casos de candidiasis vulvovaginal recurrente en mujeres no embarazadas, deben administrarse dos dosis orales de 150 mg separadas por 3 días para conseguir la remisión micológica. Después, debe seguirse un tratamiento de mantenimiento de 100-150 mg una vez por semana durante 6 meses para prevenir la recurrencia. También se recomienda una pauta de 2 dosis de fluconazol oral (dos dosis de 150 mg con 3 días de diferencia) para tratar la candidiasis vulvovaginal grave en mujeres no embarazadas.
Leishmaniasis
Se ha probado el fluconazol para tratar la leishmaniasis cutánea causada por Leishmania major. En un estudio aleatorizado, doble ciego y controlado con placebo, 80 pacientes recibieron 200 mg diarios de fluconazol oral durante 6 semanas; 63 de ellos tuvieron curación completa de las lesiones a los 3 meses, frente a 22 de 65 pacientes que recibieron placebo. Sin embargo, otros autores han descrito una tasa de respuesta no significativamente diferente de la del placebo.
Otras infecciones candidiásicas
Para tratar la candidiasis sistémica, la dosis habitual de fluconazol en adultos es de 400 mg como dosis única el primer día, seguida de 200 mg una vez al día. En un número limitado de pacientes con infecciones candidiásicas del tracto urinario y peritonitis, se han utilizado dosis de 50-200 mg al día. No se han establecido la dosis óptima ni la duración del tratamiento en pacientes con candidemia, candidiasis diseminada y neumonía; sin embargo, un número limitado de estos pacientes ha recibido dosis de fluconazol de hasta 400 mg al día. Algunos clínicos han recomendado dosis diarias de 400-800 mg en pacientes con candidiasis invasiva. El tratamiento debe mantenerse al menos 4 semanas y, además, durante al menos 2 semanas después de que desaparezcan los síntomas.
Infecciones criptocócicas
Para tratar la meningitis criptocócica, la dosis habitual de fluconazol en adultos es de 400 mg como dosis única el primer día, seguida de 200 a 400 mg una vez al día. Algunos datos sugieren que la dosis de 400 mg es más eficaz que las dosis menores para tratar esta infección. En algunos pacientes con infección por el virus de la inmunodeficiencia humana (VIH), se han utilizado dosis más altas de fluconazol (es decir, 800-1000 mg al día) para tratar la meningitis criptocócica. En el tratamiento inicial de la meningitis criptocócica, el fluconazol suele mantenerse durante 10-12 semanas después de que el líquido cefalorraquídeo sea estéril.

Coccidioidomicosis
Para tratar la meningitis coccidioidal en adultos, se han recomendado dosis de fluconazol de 200-800 mg una vez al día. En pacientes con SIDA y meningitis coccidioidal, se recomiendan dosis de 400-800 mg al día. En algunos casos se ha utilizado tratamiento concomitante con anfotericina B por vía intracisternal, intraventricular o intratecal.
Blastomicosis o histoplasmosis
Si se utiliza fluconazol para tratar la blastomicosis o la histoplasmosis, se recomienda una dosis diaria de 400-800 mg.
Prevención de infecciones fúngicas en personas con infección por VIH
Para la profilaxis primaria frente a la criptococosis en adultos o adolescentes con infección por VIH y recuentos absolutos de células T auxiliares/inductoras (CD4+, T4+) inferiores a 50/mm3, en España la práctica suele seguir las guías europeas y de expertos, según las cuales puede considerarse fluconazol oral 100-200 mg una vez al día en pacientes seleccionados.
Aunque hay algunos datos que sugieren que el fluconazol oral administrado a 400 mg una vez por semana puede ser eficaz como profilaxis primaria frente a infecciones fúngicas en personas con infección por VIH, esta pauta no figura en las recomendaciones actuales de las guías que suelen seguirse en España. Hacen falta más estudios para evaluar la eficacia de pautas distintas de la administración diaria en la profilaxis primaria.
Para el tratamiento supresor o de mantenimiento a largo plazo (profilaxis secundaria) de la coccidioidomicosis en adultos o adolescentes con infección por VIH que han tenido infecciones documentadas y tratadas adecuadamente, suele recomendarse una dosis de fluconazol de 400 mg una vez al día. Para el tratamiento supresor o de mantenimiento destinado a prevenir la recurrencia o recaída de la criptococosis en adultos o adolescentes con infección por VIH con infecciones documentadas y tratadas adecuadamente, la dosis habitual de fluconazol oral es de 200 mg una vez al día.
Algunos clínicos recomiendan que, en el tratamiento supresor a largo plazo frente a la criptococosis, el fluconazol oral se administre a una dosis de 400 mg al día durante las primeras 4 semanas, seguida de 200 mg al día. Si se utiliza fluconazol oral como tratamiento supresor o de mantenimiento a largo plazo (profilaxis secundaria) para prevenir la recurrencia o recaída de candidiasis mucocutánea (orofaríngea, vaginal, esofágica) en adultos o adolescentes con infección por VIH que han tenido episodios frecuentes o graves de estas infecciones candidiásicas, suele recomendarse una dosis de 100-200 mg una vez al día.
Aunque el fluconazol se ha administrado a dosis de 200 mg una vez por semana como tratamiento supresor a largo plazo en mujeres con infección por VIH y antecedentes de candidiasis orofaríngea o vaginal, esta pauta no se incluye en las recomendaciones de las guías vigentes que suelen seguirse en España. Existe preocupación por que este régimen favorezca la aparición de cepas de Candida resistentes a fluconazol. El tratamiento supresor o de mantenimiento a largo plazo para prevenir la recurrencia o recaída de infecciones fúngicas en pacientes con infección por VIH suele mantenerse de por vida. Sin embargo, en algunos adultos y adolescentes que hayan recuperado la inmunidad como resultado de una terapia antirretroviral combinada potente, puede ser razonable suspender el tratamiento supresor o de mantenimiento para la criptococosis.
Prevención de infecciones fúngicas en pacientes trasplantados y con cáncer
Para prevenir la candidiasis en receptores de trasplante de médula ósea, la dosis recomendada de fluconazol es de 400 mg una vez al día. En pacientes en los que se espera una granulocitopenia grave (recuento de neutrófilos inferior a 500/mm3), el tratamiento con fluconazol debe iniciarse unos días antes del comienzo previsto de la neutropenia. Debe mantenerse durante 7 días después de que el recuento de neutrófilos supere los 1000/mm3.
Dosis pediátrica
La dosis habitual de fluconazol en pacientes pediátricos varía de 3 a 12 mg/kg/día; no se recomiendan dosis superiores a 600 mg al día. El fabricante indica que una dosis diaria de 3, 6 o 12 mg/kg en pacientes pediátricos equivale a 100, 200 o 400 mg al día, respectivamente, en adultos. Algunos niños mayores pueden tener aclaramientos similares a los de los adultos.
Para tratar meningitis o septicemia causadas por Candida sensible, neonatos y lactantes de 3 meses o menos han recibido fluconazol a dosis de 5-6 mg/kg/día, administrado por vía oral o mediante perfusión intravenosa durante 1 hora. En algunos neonatos y lactantes con septicemia se administró una dosis de carga inicial de 10 mg/kg, seguida de 5 mg/kg/día. Basándose en los datos disponibles sobre la farmacocinética del fluconazol en neonatos prematuros, el fabricante recomienda que los neonatos de 2 semanas o menos reciban la misma dosis diaria que los niños mayores, pero administrada una vez cada 72 horas.
Candidiasis orofaríngea y esofágica
Para el tratamiento de la candidiasis orofaríngea o esofágica, el fabricante recomienda que los pacientes pediátricos reciban 6 mg/kg de fluconazol el primer día, seguido de 3 mg/kg una vez al día. La dosis para la candidiasis esofágica puede aumentarse hasta 12 mg/kg al día si es necesario, según la situación clínica del paciente y la respuesta al medicamento. El tratamiento de la candidiasis orofaríngea debe mantenerse al menos 2 semanas para reducir la probabilidad de recaída. El tratamiento de la candidiasis esofágica debe continuar durante al menos 3 semanas y, además, durante al menos 2 semanas después de que desaparezcan los síntomas.
Otras infecciones fúngicas
Se ha administrado fluconazol a dosis de 6-12 mg/kg/día para tratar infecciones candidiásicas sistémicas en pacientes pediátricos. El fabricante recomienda tratar la meningitis criptocócica en pacientes pediátricos con una dosis inicial de 12 mg/kg el primer día, seguida de 6 mg/kg una vez al día. Si es necesario, la dosis puede aumentarse hasta 12 mg/kg al día según la situación clínica y la respuesta al medicamento. El tratamiento con fluconazol debe continuar durante 10-12 semanas después de que el LCR dé negativo en cultivo.
Prevención de infecciones fúngicas en personas con infección por VIH
La dosis recomendada de fluconazol oral para la profilaxis primaria frente a la criptococosis en lactantes y niños con infección por VIH e inmunosupresión grave es de 3-6 mg/kg una vez al día. Si se utiliza fluconazol oral como tratamiento supresor o de mantenimiento a largo plazo para prevenir la recurrencia o recaída de criptococosis o candidiasis mucocutánea (orofaríngea, esofágica) en lactantes y niños con infección por VIH, la dosis recomendada es de 3-6 mg/kg una vez al día. Se recomienda una dosis de 6 mg/kg una vez al día para prevenir la recurrencia o recaída de la coccidioidomicosis en estos pacientes pediátricos.
Interacciones
En general, el fluconazol produce menos interacciones que el itraconazol o el ketoconazol. El uso de rifampicina con fluconazol reduce las concentraciones plasmáticas de fluconazol. La combinación de hidroclorotiazida y fluconazol ha producido aumentos clínicamente poco relevantes en las concentraciones plasmáticas de fluconazol.
El fluconazol puede interferir en el metabolismo de otros fármacos, sobre todo por inhibición de las isoenzimas CYP3A4 y CYP2C9 del citocromo P450. Esto puede explicar los aumentos descritos en las concentraciones plasmáticas de bosentán, ciclosporina, midazolam, nevirapina, amitriptilina, nortriptilina, fenitoína, rifabutina, hipoglucemiantes del grupo de las sulfonilureas y nateglinida, inhibidores selectivos de la ciclooxigenasa-2 como celecoxib y parecoxib, tacrolimus, triazolam, warfarina y zidovudina. El fluconazol puede inhibir la formación de un metabolito tóxico del sulfametoxazol. Los aumentos de las concentraciones de terfenadina tras dosis altas de fluconazol se han asociado con anomalías en el ECG.
Cabe esperar un efecto parecido con astemizol. Sin embargo, el uso de fluconazol con cisaprida podría aumentar las concentraciones de cisaprida y causar la toxicidad asociada, por lo que debe evitarse. El uso concomitante de fluconazol con astemizol, cisaprida o terfenadina debe evitarse debido al riesgo de arritmias cardiacas. Se ha atribuido un síncope al aumento de las concentraciones de amitriptilina cuando se administró junto con fluconazol.
El fluconazol también puede reducir el aclaramiento de teofilina. Se ha descrito tanto aumento como disminución de la concentración de esteroides anticonceptivos en pacientes que reciben fluconazol, y la eficacia de los anticonceptivos orales puede verse afectada. Para más información sobre las interacciones entre fármacos metabolizados por la isoenzima CYP3A del citocromo P450 y los azoles, véase el apartado de itraconazol.
Fluoroquinolonas
Tanto el levofloxacino como el fluconazol pueden prolongar el intervalo QT. El uso simultáneo de levofloxacino intravenoso y fluconazol dio lugar a un episodio de torsade de pointes en un paciente en hemodiálisis.

Interacciones microbiológicas
Se observó un efecto antifúngico sinérgico in vitro con terbinafina y fluconazol frente a cepas de Candida albicans.
Resistencia
La aparición de cepas de Candida spp. resistentes a fluconazol se ha vuelto cada vez más importante, especialmente en pacientes inmunodeprimidos que reciben profilaxis prolongada con fluconazol. Además de la resistencia en Candida albicans, en estos pacientes se han detectado infecciones por Candida dubliniensis, Candida glabrata y Candida krusei, todas ellas potencialmente menos sensibles al fluconazol que Candida albicans. También se ha descrito resistencia secundaria de Candida glabrata durante el tratamiento con fluconazol.
Se ha informado de que la resistencia al fluconazol aparece con más frecuencia que la resistencia al ketoconazol o al itraconazol, lo que podría estar relacionado con el uso generalizado del medicamento. También se ha descrito resistencia cruzada con otros azoles y con anfotericina B.
Se ha descrito resistencia al fluconazol en Cryptococcus neoformans e Histoplasma capsulatum. Se desarrolló histoplasmosis durante el tratamiento con fluconazol en un paciente con infección por VIH. Se aisló C. neoformans resistente a fluconazol en un paciente inmunocompetente no expuesto previamente a antifúngicos azólicos.
Interacciones del fluconazol con otros fármacos
Alfentanilo
En un estudio aleatorizado, doble ciego, controlado con placebo y cruzado en nueve sujetos, fluconazol 400 mg redujo el aclaramiento de alfentanilo 20 microgramos/kg en un 55 % y aumentó los efectos subjetivos inducidos por alfentanilo.
Amitriptilina
Se ha descrito una interacción entre el fluconazol y la amitriptilina.
- Un niño de 12 años con rabdomiosarcoma prostático presentó episodios periódicos de síncope durante 7 meses mientras tomaba fluconazol para la mucositis inducida por quimioterapia. Ya había tomado fluconazol antes sin problemas, pero además tomaba una dosis estable de amitriptilina para el dolor neuropático. Al suspender la amitriptilina, no volvió a presentar episodios. El efecto se confirmó al reintroducirla.
La administración conjunta de fluconazol probablemente aumenta la exposición a amitriptilina. En tres casos descritos en adultos se observaron aumentos de las concentraciones plasmáticas de amitriptilina con la administración concomitante de fluconazol; en una paciente, una mujer de 57 años, se prolongó el intervalo QT y apareció torsade de pointes.
Anfotericina
Los estudios in vitro y en animales han mostrado resultados contradictorios sobre el posible antagonismo entre los efectos del fluconazol y la anfotericina frente a especies de Candida. Sin embargo, grandes estudios aleatorizados y doble ciego, en los que se comparó fluconazol con y sin anfotericina durante 5 días en pacientes no neutropénicos con candidemia, no mostraron evidencia de antagonismo, sino una eliminación más rápida del microorganismo de la sangre y una tendencia a mejores resultados en quienes recibieron la combinación.
Antiácidos
La absorción de fluconazol tras la administración oral no se ve influida por el pH gástrico; por tanto, antiácidos como co-magaldrox no afectan a su absorción.
Antihistamínicos
El uso concomitante de terfenadina con fluconazol puede dar lugar a concentraciones peligrosamente elevadas de terfenadina y provocar cardiotoxicidad. Se sospecha que podría ocurrir lo mismo con astemizol.
Benzodiacepinas
Doce hombres sanos participaron en un ensayo aleatorizado, doble ciego y cruzado de cuatro vías para determinar la interacción de fluconazol con bromazepam. Recibieron dosis únicas orales o rectales de bromazepam (3 mg) tras un pretratamiento de 4 días con fluconazol oral (100 mg/día) o placebo. El fluconazol no produjo cambios significativos en la farmacocinética ni en la farmacodinámica del bromazepam oral o rectal.
El fluconazol aumentó las concentraciones sanguíneas de midazolam y triazolam.
Los efectos del fluconazol (dosis de carga de 400 mg seguida de 200 mg/día) sobre la cinética de midazolam se estudiaron en 10 adultos con ventilación mecánica que recibían una infusión estable de midazolam. Las concentraciones de midazolam aumentaron hasta cuatro veces tras iniciar el tratamiento con fluconazol; estos cambios fueron más marcados en pacientes con insuficiencia renal. Durante el estudio, la proporción de a-hidroximidazolam a midazolam fue disminuyendo progresivamente. Los autores concluyeron que, en pacientes de UCI que reciben fluconazol, debe considerarse reducir la dosis de midazolam si aumenta el grado de sedación.
En un estudio farmacocinético y farmacodinámico con midazolam oral 7,5-15 mg, el paso de la inhibición del metabolismo por itraconazol 200 mg/día a la inducción por rifampicina 600 mg/día causó un cambio de hasta 400 veces en el AUC de midazolam oral.
Bloqueadores de los canales de calcio
El fluconazol potenció los efectos antihipertensivos del nifedipino al aumentar sus concentraciones plasmáticas en un paciente de 16 años con feocromocitoma maligno que tomaba nifedipino de forma crónica para la hipertensión arterial y recibió fluconazol para una septicemia por Candida.
Carbamazepina
El fluconazol puede causar toxicidad por carbamazepina, presumiblemente por inhibición de CYP3A4.
- Un hombre de 33 años en tratamiento estable con carbamazepina (400 mg tres veces al día) para un trastorno convulsivo quedó estuporoso por toxicidad por carbamazepina tras recibir fluconazol 150 mg/día durante 3 días. La suspensión de ambos medicamentos hizo que descendiera la concentración de carbamazepina (máx 25 µg/ml) y el paciente recuperó su estado mental basal. La carbamazepina se reinició sin más acontecimientos adversos.
- Las concentraciones séricas de carbamazepina aumentaron durante la administración concomitante de fluconazol (400 mg/día) en un hombre de 38 años.
Ciclosporina
El fluconazol puede aumentar las concentraciones de ciclosporina por inhibición de CYP3A4. En algunos estudios se observaron efectos mínimos o nulos, pero en otros el fluconazol aumentó las concentraciones de ciclosporina. Las diferencias en la dosis y en la duración del tratamiento con fluconazol podrían explicar estas discrepancias. Por ejemplo, no hubo interacción con una dosis de fluconazol de 100 mg/día, pero las dosis altas (400 mg/día o más) aumentaron las concentraciones plasmáticas de ciclosporina y tacrolimus.
La interacción entre ciclosporina y fluconazol se evaluó retrospectivamente en 19 receptores de trasplante renal y de páncreas/riñón. Tanto el fluconazol intravenoso como el oral alteraron la concentración plasmática de ciclosporina. Cinco sujetos no tuvieron interacción significativa y 15 sí. Ningún paciente presentó nefrotoxicidad ni rechazo del trasplante relacionado con el tratamiento antifúngico.
Los efectos de dosis más altas de fluconazol sobre la inmunosupresión con ciclosporina se investigaron en seis pacientes con trasplante renal en un estudio prospectivo, abierto y cruzado. Se compararon la función renal basal, el AUC de ciclosporina, la Cmax, la Cmm, la fmax y el aclaramiento con los valores obtenidos a los 2, 4 y 7 días de iniciar fluconazol oral a 200 mg/día. A partir del día 8, se redujo la dosis de ciclosporina en un 50 % y se repitieron las mediciones el día 14. Los resultados se muestran en la Tabla 1. En el ANOVA de medidas repetidas, sólo el AUC y la Cmax en el día 4 con fluconazol fueron significativamente mayores que en el día 0. No hubo cambios significativos en el aclaramiento ni en la fmax de ciclosporina. Los autores concluyeron que los cambios en la Cmin pueden no ser lo bastante sensibles para detectar la interacción descrita y sugirieron monitorizar el AUC hacia el día 4 para orientar los ajustes de dosis de ciclosporina en todos los pacientes con fluconazol concomitante.
Cimetidina
La absorción de fluconazol tras la administración oral no se ve influida por el pH gástrico; por tanto, la cimetidina no tiene efecto.
Claritromicina
Se estudiaron los efectos de fluconazol y claritromicina sobre la farmacocinética de rifabutina y 25-O-desacetilrifabutina en 10 pacientes con infección por VIH que recibieron rifabutina 300 mg cuatro veces al día, además de fluconazol 200 mg cuatro veces al día y claritromicina 500 mg cuatro veces al día. Hubo un aumento del 76 % del AUC plasmático de rifabutina cuando se administró fluconazol o claritromicina por separado y un aumento del 152 % cuando ambos fármacos se administraron juntos. Los autores concluyeron que los pacientes deben ser vigilados para detectar efectos adversos de rifabutina cuando se coadministra con fluconazol o claritromicina.
Ciclofosfamida
La ciclofosfamida es un profármaco metabolizado por enzimas CYP450 para producir especies alquilantes, que son citotóxicas, y el grado de metabolismo de la ciclofosfamida se correlaciona tanto con la eficacia terapéutica como con la toxicidad. Estudios in vitro en seis microsomas hepáticos humanos mostraron que el IC50 del fluconazol para reducir la producción de 4-hidroxiciclofosfamida fue de 9 a 80 µmol/l.
Un estudio retrospectivo en 22 niños con cáncer analizó la posible interacción entre fluconazol y ciclofosfamida. Se seleccionó a niños con un perfil establecido de metabolismo de ciclofosfamida que no recibían otros fármacos conocidos por afectar a ese metabolismo. Nueve recibían fluconazol y 13 eran controles. El aclaramiento plasmático fue significativamente menor en los pacientes con fluconazol concomitante (2,4 frente a 4,2 l/h/m). No está claro si esta interacción reduce la eficacia terapéutica de la ciclofosfamida.
Doxorrubicina
Se investigó el efecto del fluconazol sobre la farmacocinética plasmática de doxorrubicina en un estudio cruzado y aleatorizado en primates no humanos. El fluconazol (10 mg/kg/día) se administró por vía intravenosa durante 4 días antes de la doxorrubicina (2,0 mg/kg por vía intravenosa). El pretratamiento con fluconazol no afectó a la farmacocinética de la doxorrubicina, y la incidencia de neutropenia grave (recuento absoluto de neutrófilos por debajo de 0,5 x 109/l) fue mayor con doxorrubicina sola que con la combinación de doxorrubicina y fluconazol. Por tanto, el fluconazol no parece contribuir a los efectos mielosupresores de la doxorrubicina.
Flucitosina
El uso concomitante de fluconazol y flucitosina puede tener un efecto aditivo. Esta combinación podría ayudar en el tratamiento de la meningitis criptocócica.
Inhibidores de la proteasa del VIH
La interacción farmacocinética entre fluconazol 400 mg una vez al día e indinavir 1000 mg tres veces al día se evaluó en un estudio cruzado, controlado con placebo, de 8 días; no hubo interacción significativa.
Se estudió el efecto del fluconazol sobre la farmacocinética en equilibrio estacionario de ritonavir y saquinavir en pacientes con infección por VIH-1. Recibieron el inhibidor de la proteasa (saquinavir 1200 mg tres veces al día, n=5, o ritonavir 600 mg dos veces al día) solo el día 1, y después junto con fluconazol 400 mg el día 2 y 200 mg los días 3-8. El aumento mediano del AUC de saquinavir fue del 50 %, y el aumento mediano de la Cmax fue del 56 %. En cambio, el fluconazol no afectó a la disposición de ritonavir.
Metadona
Se ha descrito una interacción entre el fluconazol y la metadona (un sustrato de CYP3A4, CYP2C9 y CYP2C).
Mientras tomaba una dosis estable de metadona, un hombre de 60 años con cáncer avanzado desarrolló depresión respiratoria 2 días después de recibir fluconazol intravenoso para una candidiasis oral refractaria. La naloxona intravenosa revirtió la depresión respiratoria.
En un estudio aleatorizado, doble ciego y controlado con placebo en 25 pacientes, fluconazol 200 mg/día aumentó las concentraciones de metadona, pero los pacientes tratados con fluconazol no presentaron signos ni síntomas de sobredosis importante de narcóticos.
Omeprazol
La absorción de fluconazol tras la administración oral no se ve influida por el pH gástrico; por tanto, el omeprazol no tiene efecto. El omeprazol se metaboliza ampliamente en el hígado mediante reacciones de 5-hidroxilación y sulfoxidación, catalizadas sobre todo por CYP2C19 y CYP3A4, respectivamente. El fluconazol es un inhibidor competitivo potente de CYP2C19 y un inhibidor débil de CYP3A4. Se evaluó el efecto del fluconazol sobre la farmacocinética de una dosis oral única de omeprazol 20 mg tras una dosis oral única de fluconazol 100 mg y después de 4 días de administración oral de 100 mg/día en 18 voluntarios varones sanos. El fluconazol aumentó la Cmax y el AUC medio de omeprazol y prolongó su vida media (2,59 frente a 0,85 horas).
Anticonceptivos orales
El fluconazol no alteró de forma significativa la farmacocinética de etinilestradiol o norgestrel, y los investigadores interpretaron que esto sugiere que el tratamiento con fluconazol en usuarias de anticonceptivos orales no aumentaría el riesgo de embarazo. Sin embargo, el estudio utilizó una dosis de 50 mg de fluconazol, y la experiencia con dosis más altas ha mostrado resultados diferentes.
En otro estudio, el fluconazol redujo la disponibilidad sistémica de etinilestradiol en un anticonceptivo oral, aunque no se describieron las dosis utilizadas.
En un estudio abierto y cruzado realizado en 10 sujetos jóvenes y sanos, fluconazol a dosis de 150 mg aumentó las concentraciones séricas de etinilestradiol administrado a dosis de 30-35 µg al día.
La posible interacción farmacocinética entre fluconazol 300 mg una vez por semana y un anticonceptivo oral que contenía etinilestradiol y noretindrona (Ortho-Novum 7/7/7; Ortho-McNeil Pharmaceutical Inc, Raritan, NJ) se estudió en un ensayo de dos vías, aleatorizado, doble ciego, cruzado y controlado con placebo en 26 mujeres sanas de 18 a 36 años. Durante el primer ciclo, tomaron solo el anticonceptivo oral. En el segundo ciclo, se las asignó aleatoriamente a anticonceptivo oral + fluconazol o anticonceptivo oral + placebo. En el tercer ciclo, recibieron el otro tratamiento.
El fluconazol produjo aumentos pequeños pero estadísticamente significativos en el AUC0-24 de etinilestradiol y noretindrona. Las pacientes que tomaron fluconazol no experimentaron acontecimientos adversos relacionados con el tratamiento.
Por tanto, parece que no hay riesgo de fallo anticonceptivo debido a la administración concomitante de fluconazol.
Fenitoína
La coadministración de fluconazol y fenitoína dio lugar a concentraciones marcadamente más altas de fenitoína.
Rifamicinas
La combinación de rifampicina con fluconazol tiene efectos insignificantes.
Estatinas
Se estudiaron los efectos del fluconazol sobre las concentraciones plasmáticas de fluvastatina y pravastatina en dos estudios separados, aleatorizados, doble ciego, de dos fases y cruzados. Voluntarios sanos recibieron fluconazol oral (400 mg el día 1 y 200 mg los días siguientes) o placebo. El día 4, recibieron una dosis oral única de fluvastatina 40 mg o pravastatina 40 mg.
El fluconazol aumentó el AUC plasmático y la vida media de la fluvastatina en un 80 %, pero no tuvo efectos significativos sobre la farmacocinética de la pravastatina. El mecanismo de la prolongación de la eliminación de fluvastatina probablemente fue la inhibición de CYP2C9. En cambio, la pravastatina parece no ser susceptible a interacciones con fluconazol y otros inhibidores de CYP2C9.
Se investigó el efecto del fluconazol sobre la farmacocinética de rosuvastatina en un estudio aleatorizado, doble ciego, cruzado de dos vías y controlado con placebo. Voluntarios varones sanos recibieron 200 mg/día de fluconazol o placebo durante 11 días; el día 8 se coadministró rosuvastatina 80 mg. Se midieron las concentraciones plasmáticas de rosuvastatina, N-desmetilrosuvastatina y los inhibidores activos y totales de HMG-CoA reductasa hasta 96 horas después de la dosis.
El fluconazol aumentó el AUC y la Cmax de rosuvastatina en un 14 % y un 9 %, respectivamente. Los pocos datos disponibles para el metabolito N-desmetilado mostraron que la Cmax disminuyó un 25 %. El fluconazol no afectó a la proporción de inhibidores activos o totales de HMG-CoA reductasa circulantes atribuida a la rosuvastatina. Por tanto, el fluconazol sólo produjo cambios menores en la cinética de la rosuvastatina, sin relevancia clínica.
Sulfonilureas
La administración concomitante de fluconazol con tolbutamida dio lugar a un aumento de sus concentraciones.
- Un paciente VIH positivo de 56 años con diabetes mellitus que tomaba gliclazida 160 mg/día desarrolló hipoglucemia grave cuando recibió cotrimoxazol 480 mg/día y fluconazol 200 mg/día. Los autores especularon que el fluconazol pudo haber inhibido el metabolismo de la gliclazida por inhibición de CYP2C9.
Se estudiaron los efectos del fluconazol y de la fluvoxamina sobre la farmacocinética y la farmacodinámica de la glimepirida en un estudio aleatorizado, doble ciego y cruzado realizado en 12 voluntarios sanos, que recibieron una vez al día durante 4 días fluconazol 200 mg/día (400 mg el primer día), fluvoxamina 100 mg/día o placebo. El cuarto día se administró una dosis única oral de glimepirida de 0,5 mg.
El fluconazol aumentó el AUC total medio de glimepirida al 238 %, el pico plasmático al 151 % respecto al control, y prolongó la vida media de glimepirida de 2,0 a 3,3 horas. Probablemente se debió a la inhibición por el fluconazol del metabolismo de glimepirida mediado por CYP2C9. Sin embargo, el fluconazol no produjo cambios estadísticamente significativos en los efectos de glimepirida sobre la glucemia.
Tacrolimus
Dado que el tacrolimus se metaboliza por CYP3A4 intestinal y hepático, los fármacos que inhiben esta enzima pueden reducir su metabolismo y aumentar sus concentraciones sanguíneas.
Se investigó el efecto del fluconazol sobre las concentraciones sanguíneas de tacrolimus en ocho pacientes con trasplante hepático a quienes se retiró el fluconazol profiláctico (200 mg/día) debido a elevación de transaminasas hepáticas, disfunción renal o eosinofilia (un caso de cada). Las concentraciones calculadas de tacrolimus descendieron entre un 13 y un 81 % (mediana del 41 %) entre el cuarto y el noveno día tras retirar el fluconazol. Deben controlarse cuidadosamente las concentraciones sanguíneas de tacrolimus y ajustar la dosis según sea necesario tras retirar el fluconazol.
La interacción entre tacrolimus y fluconazol se evaluó retrospectivamente en 19 receptores de trasplante renal y de páncreas/riñón. Tanto el fluconazol intravenoso como el oral alteraron las concentraciones sanguíneas de tacrolimus. Cinco sujetos no presentaron interacciones significativas y 15 sí. Ningún paciente presentó nefrotoxicidad ni rechazo del trasplante relacionado con el tratamiento antifúngico.
- Un hombre de 17 años con fibrosis quística que tomó itraconazol tras un trasplante de pulmón e hígado presentó concentraciones altas de tacrolimus a pesar de una dosis relativamente baja (0,1-0,3 mg/kg/día).
- Un paciente que tomaba tacrolimus 0,085 mg/kg dos veces al día con itraconazol 200-400 mg/día desarrolló cetoacidosis, neutropenia y trombocitopenia, lo que obligó a suspender ambos fármacos.
- Un receptor renal de 34 años que seguía un régimen estable de tacrolimus y metilprednisolona recibió itraconazol 100 mg dos veces al día para una infección por levaduras en las vías urinarias. El tratamiento concomitante con itraconazol provocó un marcado aumento de las concentraciones mínimas de tacrolimus al segundo día de tratamiento (de 13 a 21 µg/ml) y un aumento de la creatinina sérica, lo que hizo necesaria una reducción del 50 % de la dosis de tacrolimus.
Tras retirar el itraconazol, su efecto sobre la cinética del tacrolimus tardó 12 días en revertirse. El efecto inhibidor del itraconazol fue rápido, mientras que su desaparición fue mucho más lenta, algo importante para el manejo clínico. Por ello, durante la coadministración de itraconazol con tacrolimus es esencial una vigilancia estrecha de las concentraciones sanguíneas de tacrolimus y ajustes cuidadosos de la dosis para evitar toxicidad.
Warfarina
La administración concomitante de fluconazol y warfarina ha provocado, en algunos casos, una prolongación del tiempo de protrombina.
Zidovudina
La combinación de fluconazol con ácido valproico inhibió la glucuronidación de zidovudina in vitro en microsomas hepáticos humanos más que otros fármacos, como atovacuona y metadona.
Efectos adversos
Lea las indicaciones de uso si desea comprar fluconazol online.
Los efectos adversos descritos con fluconazol afectan con más frecuencia al aparato digestivo e incluyen dolor abdominal, diarrea, flatulencia, náuseas, vómitos y alteración del gusto. Otros efectos adversos incluyen cefalea, mareo, leucopenia, trombocitopenia, hiperlipidemias y elevación de las enzimas hepáticas. Se ha descrito hepatotoxicidad grave en pacientes con enfermedades subyacentes graves, como SIDA o neoplasias malignas. Rara vez se han descrito anafilaxia y angioedema. Las reacciones cutáneas son poco frecuentes, pero se han producido reacciones cutáneas exfoliativas, como necrólisis epidérmica tóxica y síndrome de Stevens-Johnson, con mayor frecuencia en pacientes con SIDA.
Alopecia
Se ha descrito ocasionalmente alopecia en pacientes que reciben fluconazol, especialmente durante el uso prolongado.
Efecto sobre el equilibrio de electrolitos
Se asoció hipopotasemia al uso de fluconazol en 3 pacientes con leucemia mieloide aguda.
Efectos sobre el corazón
Rara vez se han descrito prolongación del intervalo QT y torsade de pointes en pacientes que reciben fluconazol.
Efectos sobre el hígado
Aunque las reacciones hepáticas graves con fluconazol son raras, se han descrito, sobre todo en pacientes con enfermedades subyacentes graves o disfunción hepática. Son frecuentes las elevaciones de las enzimas hepáticas y también se han descrito casos de ictericia. Rara vez se ha observado necrosis hepática post mortem en pacientes con enfermedad subyacente grave que habían recibido fluconazol. En uno de estos pacientes, se concluyó que la hepatotoxicidad dependía de la dosis.

Hipersensibilidad
Se realizó con éxito una desensibilización en un paciente con SIDA que presentó hipersensibilidad tanto a fluconazol como a itraconazol. Durante 7 días se administraron dosis orales de fluconazol con aumentos graduales (empezando en 5 mg al día); después, se mantuvo una dosis de 400 mg al día. No se observaron reacciones adversas durante el periodo de desensibilización ni en los 3 meses previos a la publicación del informe.
Precauciones
Antes de comprar fluconazol online, lea la información del medicamento.
El fluconazol debe usarse con precaución en pacientes con función hepática o renal comprometida. Se han observado alteraciones en pruebas hematológicas, hepáticas y renales en pacientes con enfermedades graves subyacentes como SIDA o neoplasias malignas. Se han descrito casos raros de torsade de pointes y prolongación del QT, por lo que se recomienda precaución al administrar fluconazol a pacientes con condiciones proarrítmicas. Se ha observado teratogenicidad en animales tratados con dosis altas de fluconazol, por lo que no se recomienda durante el embarazo.
Lactancia
El fluconazol pasa a la leche materna y alcanza concentraciones similares a las del plasma materno. Sin embargo, la información autorizada del producto no recomienda su uso en mujeres en periodo de lactancia. En un caso, no se observaron efectos adversos, salvo un ligero aumento de la lactato deshidrogenasa, en un lactante expuesto al fluconazol a través de la leche materna durante 6 semanas. En España, la compatibilidad con la lactancia debe valorarse utilizando la información autorizada del producto y referencias especializadas en lactancia.
Embarazo
Se ha descrito que dosis altas (tóxicas) de fluconazol, itraconazol y ketoconazol son teratogénicas en roedores.
Aunque hay poca información sobre el uso de estos fármacos durante el embarazo en humanos, se describe el caso de una mujer que tomó fluconazol 400 mg al día durante todo el embarazo y dio a luz a un bebé con anomalías craneofaciales y de extremidades graves. Las anomalías se parecían a las asociadas con el síndrome de Antley-Bixler, un trastorno genético, pero no pudo excluirse un efecto teratogénico.
Aunque los estudios de seguimiento de prescripción con fluconazol no revelaron efectos adversos en el feto, se han producido defectos congénitos en bebés cuyas madres recibieron dosis altas de fluconazol durante 3 meses o más. Los datos recopilados por el fabricante sobre 198 mujeres expuestas a itraconazol durante el primer trimestre indicaron que la tasa de malformaciones tanto en las mujeres expuestas como en los controles coincidía con el riesgo basal esperado en la población general.
No obstante, los fabricantes recomiendan evitar fluconazol, itraconazol y ketoconazol durante el embarazo. La información autorizada indica que dosis de voriconazol equivalentes a las terapéuticas son teratogénicas y embriotóxicas en roedores. Por tanto, se recomienda evitar voriconazol durante el embarazo y que las mujeres en edad fértil utilicen anticonceptivos eficaces durante el tratamiento.
Se han hecho recomendaciones similares para posaconazol. Otros antifúngicos azólicos, incluidos butoconazol, clotrimazol, econazol, miconazol, sulconazol, terconazol y tioconazol, se han descrito como embriotóxicos pero no teratogénicos en roedores tratados con dosis altas. Muchos de estos medicamentos se usan por vía tópica o intravaginal, y la absorción sistémica por estas vías varía. Aunque estos fármacos no estén necesariamente contraindicados durante el embarazo, debe tenerse en cuenta este posible riesgo al elegir un tratamiento antifúngico para estas pacientes.














