Trematodos
Aspectos esenciales del diagnóstico
- Duela sanguínea: demostración de huevos en heces, orina o biopsia rectal
- Duela hepática: demostración de huevos en heces
- Duela intestinal: demostración de helmintos adultos o huevos en heces
- Duela pulmonar: demostración de huevos en esputo o heces
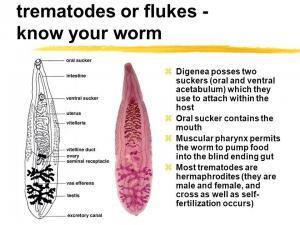
Todas las especies de trematodos que parasitan al ser humano son digenéticas. La reproducción sexual en la duela adulta va seguida de una multiplicación asexual en el estadio larvario. La mayoría de las especies de trematodos adultos presentan una ventosa oral y una ventosa ventral. Los ciclos vitales de los trematodos que son patógenos humanos importantes son similares entre las cinco especies principales. Los huevos se excretan en las heces del huésped, eclosionan en agua dulce y requieren un huésped primario en caracoles antes de que se produzca la infección en humanos. La infección por trematodos puede clasificarse en cuatro grupos generales en función del hábitat final de las duelas adultas en humanos, como sigue: duelas sanguíneas, duelas hepáticas, duelas intestinales y duelas pulmonares (Tabla 1).
Consideraciones generales
Infección por duelas sanguíneas (esquistosomiasis)
Epidemiología
Se estima que la esquistosomiasis afecta a > 200 millones de personas en todo el mundo y es endémica en Asia, África, Sudamérica y otras partes del mundo donde la población se dedica a la agricultura en agua dulce. Se estima que el número total de personas infectadas en Estados Unidos supera las 500.000, y estos casos se observan con mayor frecuencia en inmigrantes de Sudamérica, Asia y el Caribe. La enfermedad no puede propagarse en Estados Unidos porque el caracol específico que actúa como huésped intermediario aún no existe en Estados Unidos. A diferencia de la mayoría de los otros trematodos patógenos para el ser humano, los esquistosomas adultos tienen sexos separados. La duela hembra reside dentro de un surco creado por el pliegue de los bordes laterales de la duela macho.
Cada una de las cinco especies de duela sanguínea patógenas para el ser humano tiene una distribución geográfica específica, como sigue: Schistosoma mansoni, península arábiga, África, Caribe y Sudamérica; Schistosoma haematobium, Oriente Medio y África; Schistosoma japonicum, Japón, China y Filipinas; Schistosoma mekongi, Sudeste Asiático; y Schistosoma intercalatum, África occidental y central. La distribución geográfica específica depende de la presencia del caracol intermediario específico.
Microbiología y patogenia
El ciclo vital de las cinco especies principales de duelas sanguíneas es el siguiente: las duelas adultas (1-2 cm de longitud) habitan el sistema venoso del mesenterio o de la vejiga urinaria; la reproducción sexual da lugar a huevos con una forma característica, que se excretan en las heces; los huevos eclosionan en agua dulce y liberan miracidio ciliados móviles, que penetran en el cuerpo del caracol que actúa como huésped intermediario (existe un caracol específico y una distribución geográfica para cada especie de duela sanguínea); dentro del caracol, los miracidio se multiplican asexualmente y, 4-6 semanas después, emergen cientos de cercarias con cola bifurcada; las cercarias penetran en la piel humana, pierden la cola y se convierten en esquistosomas que migran a los pulmones y al hígado, donde se produce la maduración; y ~ 6 semanas después, la duela adulta madura migra a su hábitat final en los sistemas venosos. Se estima que la esperanza de vida media de las duelas adultas en humanos es de 5-10 años.
Hallazgos clínicos
Los tres estadios diferentes (cercarias, duelas maduras y huevos) de la duela sanguínea en humanos dan lugar a tres síndromes principales, en orden cronológico: dermatitis (prurito del nadador), fiebre y síntomas constitucionales (fiebre de Katayama) y, finalmente, enfermedad fibroobstructiva crónica (Tabla 2).
Signos y síntomas
La dermatitis (prurito del nadador) es la forma aguda de la esquistosomiasis y se caracteriza por un exantema pruriginoso y papular que suele aparecer en los 1-3 días posteriores a la penetración de las cercarias. El prurito del nadador rara vez se produce tras una exposición primaria y es más frecuente en personas sensibilizadas por una exposición previa.
La fiebre de Katayama aparece 4-8 semanas después de la penetración cutánea en humanos y coincide con la producción de huevos por las duelas. La fiebre de Katayama es más grave tras la infección por S japonicum, pero ocasionalmente se produce en pacientes infectados por S mansoni y rara vez por S haematobium. Los pacientes presentan un inicio agudo de fiebre, escalofríos, cefalea y tos. Los hallazgos físicos suelen incluir adenopatías y hepatoesplenomegalia. La eosinofilia es frecuente. Los síntomas suelen desaparecer en unas pocas semanas tras el inicio pero, raramente, puede producirse la muerte, por lo general asociada a infección por S japonicum. La fiebre de Katayama puede ser consecuencia de la formación de complejos inmunes por un desafío antigénico masivo debido a la exposición a los huevos de la duela.
En la esquistosomiasis fibroobstructiva crónica, el daño tisular se produce por la respuesta inflamatoria crónica a la deposición de huevos. Esto da lugar a enfermedad granulomatosa crónica y a fibrosis progresiva. El hígado y el intestino son los lugares más frecuentemente afectados en pacientes con infección causada por S mansoni, S japonicum, S mekongi o S intercalatum. Los pacientes a menudo presentan dolor abdominal crónico y diarrea. En el hígado, la fibrosis puede ocasionar hipertensión portal, hepatoesplenomegalia, varices esofágicas y hemorragia variceal. Las pruebas de función hepática suelen permanecer normales durante un periodo prolongado tras la infección. En casos crónicos no tratados, puede aparecer disfunción hepática, ictericia, ascitis e insuficiencia hepática.
En pacientes con infección por S haematobium, las duelas se localizan en el plexo vesical y se produce formación granulomatosa en la vejiga y los uréteres. La hematuria es la queja más frecuente. Con infección prolongada, pueden aparecer fibrosis, obstrucción ureteral e insuficiencia renal crónica. La frecuencia de cáncer de vejiga puede ser mayor en pacientes con infección crónica por S haematobium.
La esquistosomiasis pulmonar puede aparecer en pacientes con cirrosis hepática avanzada e hipertensión portal. El desarrollo de cortocircuitos portosistémicos permite que los huevos de la duela eludan el hígado y entren en la circulación pulmonar. Los pacientes con S haematobium también pueden desarrollar esquistosomiasis pulmonar; los huevos pueden entrar en la vena cava inferior desde el plexo vesical y alcanzar el sistema venoso pulmonar.
En pacientes con S japonicum, ~ 3% desarrolla esquistosomiasis del sistema nervioso central, que se manifiesta por lesiones ocupantes de espacio que pueden causar crisis focales. En raras ocasiones, las lesiones granulomatosas resultantes de huevos ectópicos en la vasculatura de la médula espinal pueden causar mielitis transversa.
Hallazgos de laboratorio
Los hallazgos de laboratorio más frecuentes en pacientes con esquistosomiasis incluyen eosinofilia, hematuria, anemia y - en la infección crónica terminal - pruebas de función hepática anormales, creatinina sérica elevada y uremia. El diagnóstico se establece identificando los huevos característicos de esquistosoma en las heces, la orina o una muestra de biopsia rectal. Las pruebas cutáneas o las pruebas serológicas son útiles para estudios epidemiológicos, pero no son diagnósticas de infección activa.
Diagnóstico diferencial
La esquistosomiasis hepática puede parecerse a cualquier proceso que cause hepatoesplenomegalia crónica e hipertensión portal, incluida la cirrosis alcohólica, la enfermedad de Wilson, la infección crónica por hepatitis C y muchas otras afecciones. S haematobium debe diferenciarse del cáncer de vejiga o ureteral, la enfermedad por reflujo y otros síndromes que causan hematuria o insuficiencia renal crónica.
Tratamiento
El tratamiento de los pacientes con esquistosomiasis se muestra en la Tabla 3. El praziquantel es un tratamiento seguro y eficaz para las cinco especies de Schistosoma que infectan al ser humano. Los huevos pueden eliminarse durante un tiempo tras el tratamiento, y se debe realizar un examen de heces u orina de seguimiento varios meses después de la terapia para asegurar la erradicación.
Pronóstico
El pronóstico de la esquistosomiasis es excelente en pacientes tratados antes de que se desarrolle enfermedad hepática o renal terminal. En estos pacientes, el pronóstico depende de la magnitud de la afectación del órgano diana.
Prevención
El único medio eficaz de prevención es evitar el contacto con agua dulce en áreas donde la esquistosomiasis es endémica.
Infecciones por duelas hepáticas (clonorquiasis, opistorquiasis y fascioliasis)
Consideraciones generales
El hábitat final común de las duelas hepáticas son los conductos biliares. Las duelas hepáticas que con mayor frecuencia causan infecciones humanas son Clonorchis sinensis (clonorquiasis), Opisthorchis spp. (opistorquiasis) y Fasciola hepatica (fascioliasis).
C sinensis (duela hepática china u oriental) es una duela plana y alargada (~ 15 mm x 3 mm) que habita los capilares biliares distales. Los humanos son huéspedes incidentales, y la infección es endémica en China, Hong Kong, Corea y el Sudeste Asiático. Los huevos eliminados en las heces son ingeridos por el caracol intermediario específico. Tras la ingestión, los huevos eclosionan y se convierten en miracidio. Los organismos se multiplican y producen cantidades extremadamente altas de cercarias, que salen del caracol y penetran en la piel de peces de agua dulce. Una vez que las cercarias están en la piel del pez, se enquistan como metacercarias, que son infectantes para los humanos. Los humanos y los mamíferos ictiófagos adquieren la infección por la ingestión de pescado crudo o poco cocinado que contiene metacercarias. Tras la ingestión, las metacercarias se desenquistan en el duodeno de los humanos y atraviesan la ampolla de Vater, donde las duelas maduran a adultas en los conductos biliares.
O felineus y otras especies son endémicas en el Sudeste Asiático, Europa del Este y Rusia, y son duelas hepáticas frecuentes en perros y gatos que pueden transmitirse a humanos. El ciclo vital es similar al de C sinensis.
F hepatica es una duela hepática frecuente en ovejas y ganado vacuno y es endémica en Sudamérica, Europa, África, Australia y China. Los humanos son huéspedes incidentales. Los huevos se depositan en el sistema biliar y se excretan en las heces. En agua dulce, los huevos eclosionan y los miracidio deben alcanzar y penetrar en su caracol huésped específico en un plazo de 8 h. Las cercarias emergen de los caracoles y se enquistan en plantas acuáticas y, en ocasiones, en el suelo. Las plantas son consumidas por humanos, ovejas o ganado vacuno. Los organismos se desenquistan en el duodeno. Las larvas penetran a través de la pared intestinal hacia el peritoneo, entran a través de la cápsula hepática y migran hacia los conductos biliares.
Hallazgos clínicos
La mayoría de los pacientes con infecciones por C sinensis y O felineus son asintomáticos (Tabla 2). Con infección intensa, puede producirse obstrucción biliar y colangitis. La frecuencia de colangiocarcinoma puede estar aumentada en pacientes con infección crónica por C sinensis. El diagnóstico depende de la demostración de los huevos característicos en las heces.
A diferencia de la clonorquiasis u opistorquiasis, los pacientes parasitados por F hepatica suelen ser sintomáticos, y existen dos etapas clínicas distintas de la infección. En la fase temprana, los síntomas se corresponden con la migración hepática de las larvas, y los pacientes presentan fiebre, dolor en el cuadrante superior derecho, hepatomegalia y eosinofilia. Los síntomas agudos remiten cuando las larvas entran en los conductos biliares, y la mayoría de los pacientes se vuelve asintomática en esta fase posterior de la infestación. En raras ocasiones, con infestación intensa, puede aparecer obstrucción biliar, colangitis o cirrosis biliar. El diagnóstico definitivo se realiza identificando los huevos característicos en las heces o la bilis. Una prueba serológica positiva sugiere infección. La tomografía computarizada hepática puede mostrar pequeños nódulos y trayectos tortuosos producidos por la migración de las larvas.
Diagnóstico diferencial
En la fase aguda de la infección por F hepatica, los pacientes pueden parecerse a aquellos con colangitis aguda, colecistitis, absceso hepático o infección por Neisseria gonorrhoeae (síndrome de Fitz-Hugh y Curtis). Sin embargo, la presencia de eosinofilia sugiere infección por F hepatica.
Tratamiento
El praziquantel es un tratamiento eficaz para pacientes sintomáticos con infección por C sinensis u O felineus. El bitionol es el fármaco de elección para la infección por F hepatica (Tabla 3).
Pronóstico
El pronóstico de los pacientes tratados con infección por duelas hepáticas es excelente.
Prevención
Evitar el consumo de pescado de agua dulce crudo o poco cocinado es el único medio eficaz para prevenir la infección por C sinensis u O felineus. Las personas deben evitar el consumo de plantas acuáticas y hierbas poco cocinadas en áreas donde F hepatica es endémica.
Infección por duelas intestinales (fasciolopsiasis)
Consideraciones generales
El hábitat final de las duelas intestinales es el intestino delgado. Fasciolopsis buski es endémica en el Lejano Oriente y el Sudeste Asiático. Los huevos se excretan en las heces, se desarrollan en cercarias en agua dulce y se enquistan en plantas de agua dulce. Tras el consumo humano, los organismos se desenquistan en el intestino y maduran a duelas adultas que miden 2-8 cm x 1-2 mm. Residen en la porción superior del intestino delgado, donde se adhieren a la mucosa.
Hallazgos clínicos y de laboratorio
La mayoría de los pacientes son asintomáticos, pero con infección intensa pueden aparecer dolor abdominal, diarrea y, en ocasiones, malabsorción (Tabla 2). El diagnóstico puede realizarse mediante la demostración de los huevos característicos o de duelas adultas en las heces.
Diagnóstico diferencial
La mayoría de los pacientes son asintomáticos, y el diagnóstico diferencial es el de pacientes con diarrea y dolor abdominal causados por bacterias y otros parásitos.
Tratamiento
El praziquantel es un tratamiento eficaz para las duelas intestinales (Tabla 3).
Pronóstico
El pronóstico es excelente.
Prevención
Las personas que residen en áreas endémicas deben evitar el consumo de plantas acuáticas y hierbas poco cocinadas.

Infección por duelas pulmonares (paragonimiasis)
Consideraciones generales
Paragonimus westermani es endémico en el Lejano Oriente, el subcontinente indio, Centro y Sudamérica y África occidental. Las duelas pulmonares humanas producen huevos en el esputo, que se degluten, se excretan en las heces y maduran en agua dulce a miracidio, que penetran en caracoles. Las cercarias maduras salen del caracol, penetran en cangrejos de río y cangrejos de agua dulce, y se enquistan. La infección en humanos se produce tras la ingestión de crustáceos de agua dulce crudos, poco cocinados o encurtidos. Tras la ingestión, los organismos se desenquistan en el duodeno, penetran a través de la pared intestinal, entran en la cavidad peritoneal, atraviesan el diafragma hacia el espacio pleural y entran en los pulmones, donde maduran a duelas que miden 7-15 mm x 5-8 mm. Los huevos ectópicos en el cerebro pueden producir lesiones ocupantes de espacio y crisis focales.
Hallazgos clínicos
Muchos pacientes con infección mínima a moderada son asintomáticos (Tabla 2). En infecciones agudas, los pacientes sintomáticos presentan tos productiva con esputo marrón o hemoptisis y eosinofilia. La infección intensa no tratada puede progresar a bronquitis crónica o bronquiectasias con producción de esputo de gran volumen, dolor torácico pleurítico, derrame pleural y absceso pulmonar. El diagnóstico se realiza identificando los huevos característicos en el esputo o las heces. Una serología positiva puede ser útil en el diagnóstico de infección ectópica. El diagnóstico también debe sospecharse en personas que no residen en áreas endémicas, pero tienen antecedentes de consumo de crustáceos poco cocinados importados de áreas endémicas.
Diagnóstico diferencial
La paragonimiasis pulmonar se parece a una infección bacteriana crónica, una infección micobacteriana o un carcinoma de pulmón. La presencia de eosinofilia en estos pacientes que residen en un área endémica o han viajado a ella debe sugerir el diagnóstico de paragonimiasis.
Tratamiento
El praziquantel es un tratamiento eficaz (Tabla 3).
Pronóstico
El pronóstico es excelente en pacientes tratados antes del desarrollo de bronquitis crónica o bronquiectasias.
Prevención
Las personas deben evitar el consumo de crustáceos de agua dulce crudos o poco cocinados procedentes de áreas donde P westermani es endémico.
|
Tipo |
Infección |
Especies |
Primario |
Secundario |
Localización parasitaria en humanos |
|---|---|---|---|---|---|
|
Sangre |
Esquistosomiasis |
S mansoni |
Caracoles |
Ninguno |
Venas mesentéricas inferiores |
|
Hígado |
Clonorquiasis |
C sinensis |
Caracoles |
Pescado |
Conductos biliares |
|
Intestinal |
Fasciolopsiasis |
F buski |
Caracoles |
Plantas de agua dulce |
Intestino delgado |
|
Pulmón |
Paragonimiasis |
P westermani |
Caracoles |
Cangrejos y cangrejos de río |
Pulmones |
|
Trematodo |
Más frecuente |
Menos frecuente |
|---|---|---|
|
Duelas sanguíneas |
|
|
|
Duelas hepáticas |
|
|
|
Duelas intestinales |
|
|
|
Duelas pulmonares |
|
|
|
Especie |
Primera elección |
Segunda elección |
|---|---|---|
|
S mansoni |
Praziquantel, 20 mg/kg dos veces al día durante 1 día |
Oxamniquine, 15 mg/kg dosis única. Infección adquirida en África, 20 mg/kg al día durante 3 días |
|
S haematobium |
Praziquantel, 20 mg/kg dos veces al día durante 1 día |
Metrifonate, 7,5 mg/kg dosis única, semanal durante 2 semanas |
|
S intercalatum |
Praziquantel, 20 mg/kg dos veces al día durante 1 día |
No hay un tratamiento alternativo satisfactorio |
|
S japonicum |
Praziquantel, 20 mg/kg tres veces al día durante 1 día |
No hay un tratamiento alternativo satisfactorio |
|
C sinensis |
Praziquantel, 25 mg/kg tres veces al día durante 1 día |
No hay un tratamiento alternativo satisfactorio |
|
F hepatica |
Bithionol 30-50 mg/kg en días alternos durante 10-15 dosis (dosis máxima, 2 g/día) |
No hay un tratamiento alternativo satisfactorio |
|
F buski |
Praziquantel, 25 mg/kg tres veces al día durante 1 día Praziquantel, 25 mg/kg tres veces al día durante 2 días |
No hay un tratamiento alternativo satisfactorio |

















