Especies de Shigella
Aspectos esenciales del diagnóstico
- La enteritis causada por especies de Shigella puede ser acuosa (Shigella sonnei, Shigella boydii) o disentérica (Shigella dysenteriae, Shigella flexneri).
- Los factores de riesgo incluyen la ingesta de alimentos o agua contaminados por materia fecal, así como el contacto con personas infectadas.
- El diagnóstico definitivo requiere el aislamiento microbiológico y la identificación de especies de Shigella, o la evidencia molecular de infección.
Consideraciones generales
Epidemiología
La disentería es una enfermedad ancestral y ha sido descrita a lo largo de los siglos. No fue hasta el siglo XIX cuando se reconoció que la disentería podía estar causada por amebas parasitarias o por ciertas bacterias. En 1898, Shiga reconoció y aisló bacterias de pacientes con disentería que se aglutinaban al exponerse al suero del paciente. En la actualidad, los agentes bacterianos más reconocidos de la disentería son las especies de Shigella y EIEC (véase arriba).

Las especies de Shigella son únicas entre los patógenos entéricos bacterianos, ya que < 200 y posiblemente = 10 organismos pueden atravesar la barrera del ácido gástrico y causar enfermedad. Por esta razón, la transmisión de persona a persona es frecuente. La transmisión de persona a persona se asocia con un aumento de la frecuencia de shigelosis en guarderías, colegios y centros de cuidados asistenciales. La enfermedad es más frecuente en lactantes y niños pequeños, y a menudo se presenta en familiares de los pacientes. La incidencia máxima se produce en verano, y se cree que las moscas domésticas comunes contribuyen a la diseminación de la enfermedad. También se han producido brotes por alimentos contaminados por materia fecal. La transmisión a través de agua contaminada es más frecuente en países en desarrollo que carecen de sistemas adecuados de alcantarillado y tratamiento del agua.
En Estados Unidos, S sonnei es la especie de Shigella que se detecta con mayor frecuencia, mientras que S boydii tiene distribución mundial. La prevalencia de las shigelas parece ser cíclica, con el reemplazo de la cepa predominante aproximadamente cada 20 años. Este ciclo de prevalencia es presumiblemente secundario a la inmunidad de rebaño adquirida lentamente en una población hospedadora determinada. La shigelosis epidémica, causada por S dysenteriae y S flexneri, es prevalente en países subdesarrollados, pero puede desarrollarse en cualquier lugar donde existan pobreza, hacinamiento o condiciones de guerra.
Microbiología
Shigella son bacilos gramnegativos, no móviles, anaerobios facultativos, estrechamente relacionados con el género Escherichia. Al menos 40 serotipos componen cuatro grupos o especies. Estos son S dysenteriae (serogrupo A), S flexneri (serogrupo B), S boydii (serogrupo C) y S sonnei (serogrupo D).
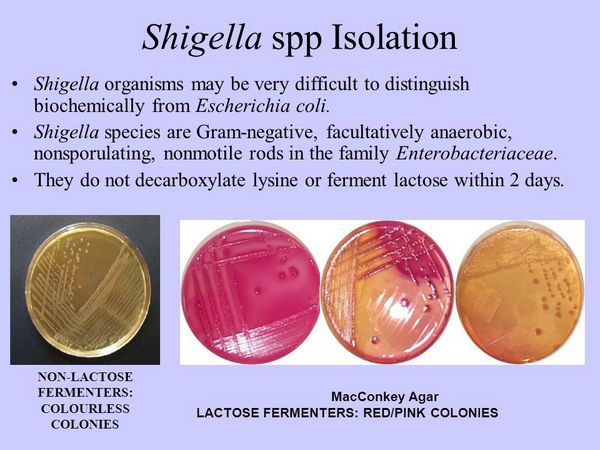
El número de shigelas presente en las heces varía según el curso de la enfermedad. Al principio, en la fase de diarrea acuosa, las shigelas son abundantes, y se cuentan 103-109 shigellae/g de heces. Durante esta fase, las shigelas se recuperan fácilmente en agar MacConkey o en agar eosina-azul de metileno (EMB), donde aparecen como colonias no fermentadoras de lactosa. Más adelante en el curso de la enfermedad, en las fases disentérica y posconvaleciente, los recuentos bacterianos en las heces descienden a 102-103 shigellae/g de heces. Además, la recuperación de shigelas es inversamente proporcional al tiempo de transporte de la muestra, especialmente en muestras de heces con un bajo número de shigelas. Durante esta última fase, el cultivo se realiza mejor mediante el transporte rápido de la muestra o la siembra del medio a pie de cama, combinado con el uso de caldo de enriquecimiento y medios de moderada a alta selectividad, como el medio xilosa-lisina-desoxicolato y el medio Shigella-Salmonella.
En muchos laboratorios, las colonias sospechosas no fermentadoras de lactosa se cribanan utilizando un conjunto de tres tubos: (i) un tubo que contiene triple sugar iron (TSI) o Kligler iron agar (KIA), (ii) un segundo tubo que contiene lysine iron agar (LIA) y (iii) un tercero que contiene Christensen's urea agar (CU) (véase también la sección de Microbiología de Salmonella más abajo). En TSI y KIA, las shigelas producen de forma característica una pendiente alcalina y un fondo ácido sin producción de gas. Aislados raros pueden producir gas. En LIA y CU se obtienen reacciones negativas, porque las shigelas no descarboxilan lisina ni hidrolizan la urea. Además, las shigelas no producen sulfuro de hidrógeno, que se detecta con los sistemas TSI, KIA y LIA. Se puede intentar aglutinar organismos que se consideren representativos de especies de Shigella mediante el uso de antisueros de grupo. Los aislamientos con un perfil de cribado sugestivo se caracterizan con mayor detalle mediante reacciones bioquímicas adicionales en sistemas tradicionales o automatizados.
Entre las pistas útiles para la identificación de las shigelas se incluyen las siguientes: la mayoría de las shigelas no pueden fermentar mucato, no pueden utilizar acetato y son negativas para indol y orto-nitrofenil-ß-galactopiranósido.
Patogenia
La shigelosis puede producir diarrea predominantemente acuosa, o diarrea acuosa que progresa a disentería. La gravedad de la enfermedad está determinada en gran medida por el organismo invasor. S dysenteriae y S flexneri son los agentes que se asocian con mayor frecuencia con la disentería bacilar, mientras que las otras especies de Shigella producen con mayor frecuencia diarrea acuosa.
La patogenia de la fase de diarrea acuosa de la disentería bacilar se debe a una combinación de replicación bacteriana luminal e invasión superficial de la mucosa en el intestino delgado. Durante esta fase, hay grandes cantidades de shigelas presentes en la luz del intestino delgado. Esta fase de la enfermedad se correlaciona con la aparición de dolor abdominal tipo cólico, fiebre y toxemia.
En cuestión de días, el contenido luminal del intestino delgado deja de contener shigelas y el sitio de infección pasa a ser el colon. Las shigelas invaden la mucosa colónica y, en ocasiones, alcanzan la submucosa. Los factores importantes para la invasión están presentes en el cromosoma bacteriano, así como en un plásmido de 140 MDa. Con el tiempo, se produce la muerte de las células epiteliales y la mucosa se desprende, posiblemente de forma secundaria a la producción de shigatoxina. La pérdida de mucosa provoca una intensa respuesta inflamatoria y permite la introducción de bacterias coliformes. Pueden observarse microabscesos, ulceraciones epiteliales y pseudomembranas que consisten en células epiteliales desprendidas, bacterias, fibrina y células inflamatorias. Esta fase de la enfermedad se correlaciona con tenesmo y deposiciones fraccionadas, de pequeño volumen, que contienen sangre, moco y restos inflamatorios.
Hallazgos clínicos
Signos y síntomas
Al inicio del curso de la enfermedad, cuando las bacterias están presentes en el intestino delgado, los pacientes desarrollan diarrea aguda acuosa, fiebre y dolor abdominal. Los pacientes pueden volverse tóxicos y la fiebre puede alcanzar hasta 40°C (104°F). Más adelante en el curso de la enfermedad, el sitio principal de infección es el colon. En esta fase, la fiebre continúa, pero suele ser menos marcada. El dolor presente suele localizarse en los cuadrantes abdominales inferiores. Las heces se vuelven disentéricas y consisten en una mezcla de neutrófilos, sangre, moco y detritus. Pueden producirse deposiciones frecuentes, de pequeño volumen o fraccionadas, y a menudo hay tenesmo. Los pacientes presentan dolor a la exploración rectal. La colonoscopia muestra mucosa colónica hiperémica, friable y con ulceración.
Diagnóstico diferencial
Cuando predomina la diarrea acuosa, deben considerarse otros patógenos entéricos bacterianos, parasitarios y víricos. Entamoeba histolytica y EIEC también deben considerarse en pacientes con disentería. La infección por E histolytica se asocia con mayor frecuencia con viajes a, o residencia en, localidades endémicas. Estos organismos se reconocen fácilmente en un examen microscópico de las heces para huevos y parásitos. Sin embargo, la disentería causada por EIEC puede plantear un desafío diagnóstico para el microbiólogo clínico. EIEC, a diferencia de otras E coli, suelen ser no móviles, pueden no fermentar lactosa o fermentarla lentamente, son negativas para la descarboxilasa de lisina y pueden reaccionar de forma cruzada con antisueros contra Shigella. El personal de laboratorio debe reconocer esta posible trampa y descartar este organismo mediante pruebas adicionales (véase arriba).
También deben considerarse causas no infecciosas de diarrea. El diagnóstico diferencial de la colitis no infecciosa es amplio e incluye enfermedad inflamatoria intestinal, colitis linfocítica/colagenosa, neoplasias y muchos otros trastornos. Los pacientes con enfermedad inflamatoria intestinal también pueden tener leucocitos fecales, lo que limita la utilidad de esta prueba. Un diagnóstico preciso puede lograrse mediante una anamnesis y exploración física exhaustivas, la exclusión de patógenos entéricos mediante estudios microbiológicos apropiados y la obtención y revisión de biopsias gastrointestinales por endoscopia y estudios histopatológicos.
Complicaciones
Las complicaciones más comunes de la disentería bacilar incluyen deshidratación y una enteropatía perdedora de proteínas. En casos raros puede producirse un megacolon tóxico, que puede resultar en perforación, hemorragia intraabdominal, peritonitis y, posiblemente, la muerte. Algunos pacientes, en particular aquellos con fenotipo HLA-B27, pueden desarrollar artritis postinfecciosa o síndrome de Reiter.
Diagnóstico
Los pacientes con diarrea aguda, que puede variar desde acuosa hasta disentérica, fiebre, dolor abdominal y sintomatología sistémica/toxemia pueden presentar shigelosis. Los antecedentes de exposición a personas con shigelosis, viajes a áreas endémicas y exposición a una población de alto riesgo, como personas en un centro de cuidados asistenciales, deben aumentar el índice de sospecha. La presencia de leucocitos en las heces, aunque es un hallazgo de apoyo, no es en modo alguno definitiva de shigelosis. Los leucocitos fecales pueden estar presentes en las heces de pacientes con otras enteritis bacterianas, disentería amebiana, colitis pseudomembranosa y enfermedades no infecciosas, como la enfermedad inflamatoria intestinal. El diagnóstico definitivo requiere la identificación microbiológica de una especie de Shigella.
Las shigelas son particularmente susceptibles a algunos cambios ambientales y mueren rápidamente durante el transporte. Por lo tanto, es imperativo transportar con rapidez las heces de los pacientes con sospecha de shigelosis al laboratorio. Esto es especialmente importante en los pacientes en fases tardías de la enfermedad, en los que el número de shigelas en las heces es relativamente bajo.
Cuando estén disponibles, las pruebas moleculares pueden complementar el cultivo de heces y aumentar la detección en pacientes que consultan tarde en el curso de la enfermedad o que ya han recibido antibióticos.
Tratamiento
El reemplazo de líquidos y electrólitos es necesario en pacientes con deshidratación. En la mayoría de los casos, esto se logra fácilmente con rehidratación oral. A diferencia de muchas otras enteritis bacterianas, la terapia antibiótica es importante en el tratamiento de la shigelosis. La antibioticoterapia limita el curso clínico de la enfermedad, puede disminuir la probabilidad de complicaciones intestinales y reduce la excreción fecal de organismos patógenos viables, lo que a su vez disminuye la transmisión. Las fluoroquinolonas son el tratamiento de elección en adultos. TMP/SMX es el tratamiento de elección en niños. Las alternativas son ampicilina, cloranfenicol y ácido nalidíxico. En áreas con resistencia conocida a TMP/SMX, como partes del sudeste asiático, África y Sudamérica, deben utilizarse quinolonas en adultos y una de las alternativas mencionadas anteriormente en niños con shigelosis. Cuando esté disponible, el perfil de susceptibilidad antimicrobiana debe guiar la terapia.
No deben utilizarse agentes antimotilidad, como difenoxilato. La inhibición de la diarrea aumenta el contacto entre la mucosa intestinal y los organismos patógenos y sus toxinas, y puede provocar una enfermedad más fulminante.
En todos los casos, la elección del antimicrobiano debe tener en cuenta los patrones locales de resistencia y factores individuales, incluidos la edad, las comorbilidades, el estado de embarazo y los antecedentes de alergia a fármacos.
| Grupo de pacientes / escenario | Terapia preferida | Alternativas y notas |
|---|---|---|
| Adultos | Fluoroquinolonas (tratamiento de elección) | Utilizar los resultados de susceptibilidad antimicrobiana cuando estén disponibles. Las alternativas incluyen ampicilina, cloranfenicol o ácido nalidíxico cuando las quinolonas están contraindicadas o no son adecuadas. |
| Niños | TMP/SMX (tratamiento de elección) | Si existe resistencia a TMP/SMX, utilizar una de las alternativas listadas (ampicilina, cloranfenicol o ácido nalidíxico) según proceda y guiado por las pruebas de susceptibilidad. |
| Regiones con resistencia conocida a TMP/SMX (por ejemplo, partes del sudeste asiático, África, Sudamérica) | Adultos: fluoroquinolonas | Niños: ampicilina, cloranfenicol o ácido nalidíxico, seleccionados según los datos locales de resistencia y la respuesta clínica. |
Pronóstico
El pronóstico es, por lo general, bueno en pacientes con shigelosis endémica o esporádica. Los lactantes y las personas mayores, especialmente si están desnutridos, presentan la mayor mortalidad. La shigelosis epidémica causada por S dysenteriae, sin embargo, es una enfermedad grave y a menudo potencialmente mortal, con tasas de mortalidad del 5% al 20%. Esta enfermedad debe tratarse de forma agresiva con antimicrobianos y terapias de rehidratación.
Prevención y control
El desarrollo y la mejora de los sistemas de eliminación de aguas residuales y de tratamiento del agua potable son importantes en los países en desarrollo. Tanto en países desarrollados como en desarrollo, la higiene personal, el correcto lavado de manos y unas condiciones de vida limpias son medidas preventivas importantes, especialmente en centros de cuidados asistenciales. El control de moscas y las prácticas higiénicas en la preparación de alimentos también deberían disminuir la incidencia de la enfermedad.
Dado que la dosis infecciosa es baja y la propagación de persona a persona es eficiente, incluso mejoras modestas en la higiene y el saneamiento ambiental pueden reducir sustancialmente la transmisión en entornos de alto riesgo.
| Ámbito | Medidas principales | Ejemplos |
|---|---|---|
| A nivel comunitario y municipal | Agua segura y gestión de aguas residuales | Mejora de la eliminación de aguas residuales, sistemas fiables de tratamiento de agua potable y protección de las fuentes de agua frente a la contaminación fecal. |
| Hogares y centros de cuidados asistenciales | Higiene personal y limpieza ambiental | Lavado regular de manos con jabón, manejo cuidadoso de pañales y residuos, limpieza rutinaria de superficies compartidas y minimizar el hacinamiento cuando sea posible. |
| Control de alimentos y vectores | Manipulación segura de alimentos y control de moscas | Lavado exhaustivo de manos antes de la preparación de alimentos, mantener los alimentos cubiertos, cocción y almacenamiento adecuados, y reducción de los sitios de cría de moscas domésticas alrededor de cocinas y letrinas. |

















